Theo các nhà nghiên cứu của Trường Đại học Dược thuộc Đại học Cardiff của Vương quốc Anh, họ vừa tìm ra một phương pháp mới không độc hại để phân phối thuốc chống ung thư đến các cơ quan của cơ thể và giảm thiểu tác dụng phụ nghiêm trọng khi sử dụng nhiều liệu pháp điều trị ung thư khác.
Phương pháp này liên quan đến việc sử dụng một loại ống nano mới – là một ống nhỏ có nhiều ứng dụng, bao gồm cả việc phân phối thuốc. Loại ống nano mới này, được thiết kế và chế tạo bởi Tiến sĩ Ben Newland tại Đại học Cardiff, được làm từ một polyme không độc hại là poly (ethylen glycol).
Trong nghiên cứu này, lần đầu tiên, họ đã tiến hành polyme hóa dưới tác dụng của ánh sáng poly(ethylene glycol) diacrylat (PEGDA) và các monome diacrylat khác trong các lỗ của khung nhôm oxid đã bị anod hóa (AAO – anodized aluminum oxide) để tạo ra các ống nano polyme. Ba ống nano polymer khác nhau (ở đây gọi là PEG, Phos và Bisphenol) được tổng hợp thành công qua quá trình polyme hóa dưới tác dụng ánh sánh của ba monome divinyl khác nhau lần lượt là: poly (ethylen glycol) diacrylat (PEGDA), bis [2- (methacryloyloxy) ethyl] phosphat và bisphenol A ethoxylat diacrylat. Các dung dịch tiền chất chứa monome divinyl và chất khởi đầu phản ứng quang hóa 2-hydroxy-2-methylpropiophenon được pha trong aceton và được thêm vào các màng xốp AAO. Các monome đã được đưa vào khung thành công, hình thành một lớp bên trong liên tục trên thành các lỗ xốp của khuôn AAO (kích thước lỗ xốp = 224 nm ± 44 nm). Sau đó, chúng được polyme hóa thành một ống nhờ các liên kết chéo khi được chiếu xạ bằng ánh sáng tia cực tím và được tách ra thông qua quá trình hòa tan khung (30 phút trong môi trường NaOH).
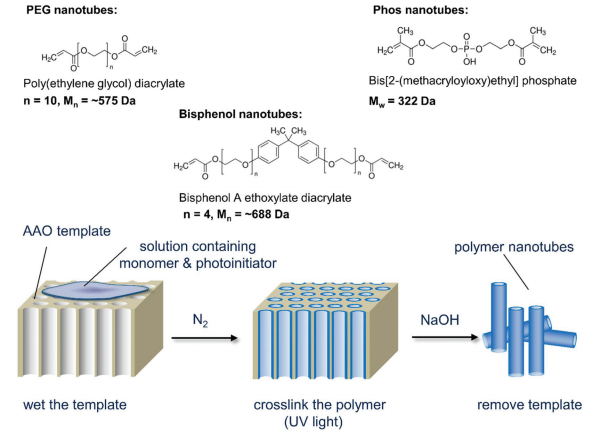
Hình 1. Mô tả phương pháp tạo ra polymer nanotubes

Hình 2. (a) Hình ảnh SEM của khung AAO, (b) Hình ảnh ống nanotube PEG (độ phóng đại cao),
(c) Hình ảnh độ phóng đại thấp của các ống nano khác nhau
Không giống như ống nano hiện tại, có thể gây ra độc tính, ống nano mới này mềm dẻo, linh hoạt và tương thích sinh học, do đó chúng dung nạp tốt bởi cơ thể.
Người ta cho rằng,các ống nano mới này không những cung cấp một phương pháp tốt hơn để phân phối thuốc chống ung thư, mà nó còn ít gây tác dụng phụ hơn đối với cơ thể.
Đó là bởi vì, hiện nay, nhiều loại thuốc được sử dụng trong hóa trị liệu các dạng ung thư khác nhau được dùng bằng đường tiêm. Mặc dù những loại thuốc này có thể tiếp cận các tế bào ung thư, nhưng chúng cũng tác động tiêu cực đến các tế bào hoàn toàn khỏe mạnh gây ra các tác dụng phụ nghiêm trọng bao gồm rụng tóc, nôn mửa và mệt mỏi.
Trong khi đó, các ống nano mới có thể được tiêm vào một bộ phận xác định của cơ thể, nghĩa là các bộ phận còn lại của cơ thể hầu như không bị ảnh hưởng bởi các thuốc chống ung thư độc hại. Để khám phá thêm điều này, nhóm đã tiến hành nghiên cứu xem liệu ống nano mới này có hiệu quả như thế nào trong điều trị ung thư vú. Một loại thuốc với tên gọi là doxorubicin đã được thử nghiệm.
Để đánh giá độc tính của ống nano khi chứa hoặc không chứa doxorubicin, hai dòng tế bào ung thư vú người đã được sử dụng: tế bào MCF-7 đáp ứng estrogen và tế bào MDA-MB-231 âm tính với ba thụ thể hormon. Kết quả cho thấy ở tế bào MCF-7 thì ống nano PEG bao gói doxorubicin ở nồng độ 60 μg/mL đã làm giảm khả năng sống của tế bào xuống 71% và 38% tương ứng sau một ngày và ba ngày. Còn đối với tế bào MDA-MB-231 thì ống nano PEG bao gói doxorubicin ở nồng độ 60 μg/ mL đã làm giảm khả năng sống của tế bào xuống 64% và 18% tương ứng sau một ngày và ba ngày.
Để kiểm chứng luận điểm rằng ống nano PEG có thể được sử dụng để kéo dài khả năng giải phóng dược chất hoặc giải phóng dược chất tại chỗ, mô hình chuột mang khối u gần (orthotopic mouse model) với chuột mang khối ung thư vú di căn cấp tính đã được đánh giá trong vòng 6 tuần (Hình 3).
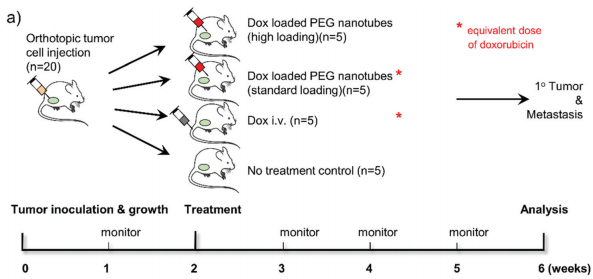
Hình 3: Hình ảnh minh họa thiết kế thí nghiệm mô tả thời gian và các nhóm chuột nghiên cứu
Kết quả cho thấy, thông qua tín hiệu phát quang sinh học liên quan đến khối u (do tế bào MDA-MB-231 gây khối u ở chuột có khả năng tiết gen mã hóa sinh tổng hợp enzym luciferase phát quang), tín hiệu của nhóm không điều trị và nhóm doxurubicin tiêm tĩnh mạch là giống nhau trong suốt 6 tuần nghiên cứu. Về kích thước khối u, với liều doxorubicin tiêm tĩnh mạch (80 µg) đã làm giảm khối lượng khối u vú ở chuột trung bình từ 549 mg ± 326 đến 414 mg ± 124, liều doxorubicin chuẩn được bao gói trong ống nano (2 khối u x 40 µg/khối u) đã làm giảm khối lượng khối u trung bình xuống 343 mg ± 111. Liều cao doxorubicin được bao gói trong ống nano (2 khối u x 80 µg/khối u) đã làm giảm đáng kể khối lượng u trên chuột (xuống 159 mg ± 64) khi so sánh với nhóm chuột chứng âm không được tiêm doxorubicin. Ngoài ra kết quả xâm lấn tự nhiên trên dòng tế bào ung thư MDA-MB-231 cho phép chúng ta phân tích khả năng di căn trên não, phổi, gan, xương cho thấy rằng điều trị cục bộ các khối u vú sơ cấp với các ống nano được nạp với liều doxorubicin chuẩn làm giảm rõ rệt di căn gan và phổi khi so sánh với doxorubicin tiêm tĩnh mạch chuột (Hình 4).
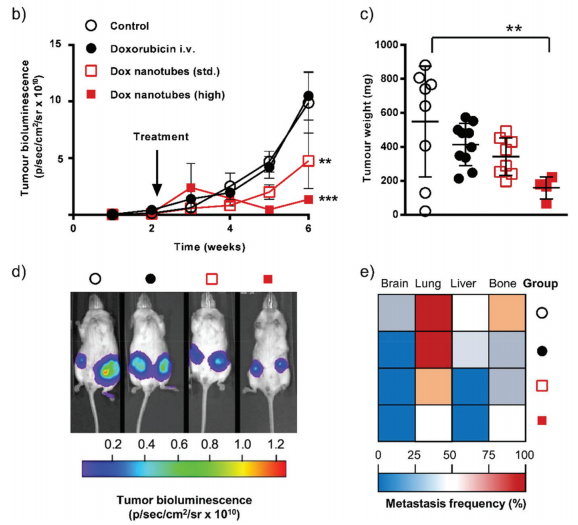
Hình 4. (b) Sự phát triển của khối u thông qua tín hiệu phát quang sinh học ở chuột: nhóm chứng (vòng tròn hở), nhóm tiêm tĩnh mạch doxorubicin 80µg (vòng tròn đen), nhóm tiêm ống nano chứa doxoruicin (2 khối u x 40 µg/khối u, hình vuông hở), nhóm tiêm ống nano chứa doxoruicin (2 khối u x 80 µg/khối u, hình vuông đỏ); (c) Khối lượng khối u chính ở thời điểm kết thúc nghiên cứu (tuần thứ 6); (d) Các hình ảnh phát quang sinh học đặc trưng cho tế bào ung thư ở tuần thứ 6; (e) Sự di căn của tế bào ung thư đến các cơ quan khác ở tuần thứ 6 (n=4).
Kết quả cho thấy phương pháp sử dụng ống nano đã làm giảm tỷ lệ di căn và tốc độ phát triển khối u, điều này cho phép nhóm nghiên cứu hy vọng về sự phát triển của loại ống nano mới này có thể đưa đến liệu pháp điều trị ung thư hiệu quả hơn trong tương lai.
Tài liệu tham khảo:
- https://phys.org/news/2018-04-method-anti-cancer-drugs.html#nRlv
- Ben Newland et al. (2016), Preparation, loading, and cytotoxicity analysis of polymer nanotubes from an ethylene glycol dimethacrylate homopolymer in comparison to multi-walled carbon nanotubes, Journal of Interdisciplinary Nanomedicine, 1 (1), pp. 9-18,doi: 10.1002/jin2.7
- Ben Newland et al. (2018), Soft and flexible poly(ethylene glycol) nanotubes for local drug delivery, Nanosacle, DOI: 10.1039/c8nr00603b.
Tổng hợp
Lê Hoàng Hảo
- Awiqli (Insulin Icodec): Giải pháp insulin nền mỗi tuần một lần dành cho bệnh nhân đái tháo đường
- Vai trò của dược sĩ trong tiêm chủng người lớn – Thực trạng, rào cản và chiến lược tiếp cận
- Ức chế PCSK9 trong dự phòng tim mạch nguyên phát – Bằng chứng mới từ thử nghiệm VESALIUS-CV
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
