Sau những nghiên cứu về các chất hoạt động chứa oxy/gốc tự do oxi hóa -reactive oxygen species (ROS) – và các chất hoạt động chứa nitơ – reactive nitrogen species (RNS), các chất hoạt động chứa lưu huỳnh – reactive sulfur species (RSS) đang được nhiều viện, trung tâm trên thế giới tập trung nghiên cứu. Trong đó, hydropersulfide (RSSH) nổi lên là chất có vai trò bảo vệ đặc biệt cho cơ thể.
RSS và RSSH là gì?
Các chất hoạt động chứa lưu huỳnh hay Reactive Sulfur Species, hiện nay, vẫn còn là khái niệm mới ở Việt Nam. Khái niệm “Reactive Sulfur Species” được chính thức chú ý vào năm 2001 khi GI. Giles đưa ra giả thuyết: vai trò của Reactive Sulfur Species trong mất cân bằng oxi hóa khử. Theo định nghĩa mới nhất, RSS là những phân tử có chứa ít nhất một nguyên tử lưu huỳnh có hoạt tính oxi hóa khử hoặc nhóm chức có chứa lưu huỳnh trong cấu trúc và có khả năng oxy hóa hoặc khử các phân tử sinh học để kích hoạt hoặc phát sinh một đáp ứng truyền tin tế bào đáng kể hoặc sinh học rộng lớn hơn. Để gọn hơn, RSS, theo chúng tôi đề xuất, là các chất hoạt động chứa lưu huỳnh, ví dụ như sulfenic acid RSOH, disulfide (R1SSR2), polysulfide (RS(S)nSR), hydropersulfide RSSH, hydropolysulfide (RS(S)nSH)…
Như vậy, RSSH là những chất hoạt động chứa lưu huỳnh và trong cấu trúc chứa thành phần –S-S-H. Những hoạt chất này như cysteine hydropersulfide (Cys-SSH), glutathione hydropersulfide (GSSH) và protein hydropersulfides (protein-SSH) được phát hiện gần đây có trong huyết tương, tế bào và mô của động vật có vú và con người. Do RSSH xuất hiện ở nồng độ thấp, hoạt tính cao, rất kém bền là những rào cản cho các nhà nghiên cứu.
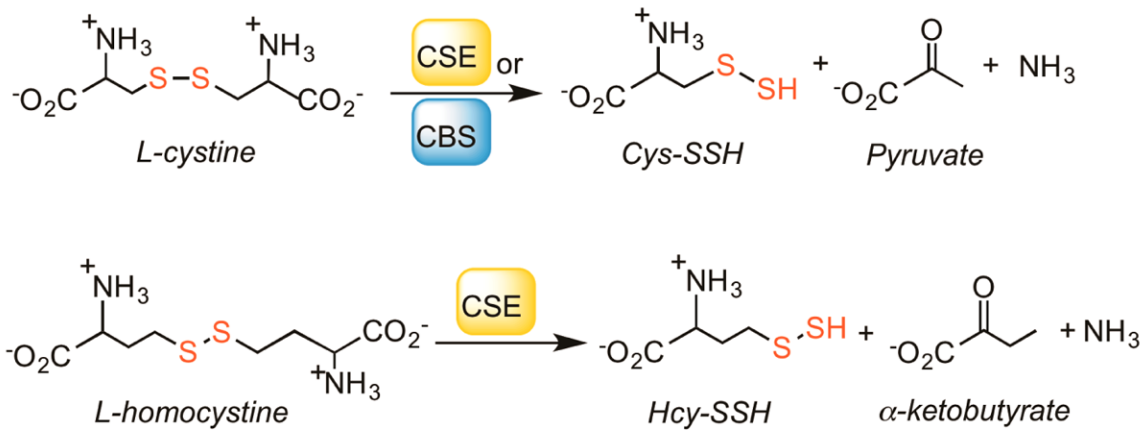
Sự hình thành các RSSH trong cơ thể (sự hình thành Cys−SSH từ cystine và enzym CBS hoặc CSE và Hcy−SSH từ homocystine và enzym CSE).
Vai trò của RSSH
ROS và RNS ở nồng độ thấp đóng vai trò quan trọng trong việc liên lạc, điều chỉnh các chức năng của tế bào và cân bằng nội môi. Tuy nhiên, khi nồng độ vượt qua giới hạn cân bằng, các thành phần này, do hoạt tính rất cao, sẽ phản ứng với các phân tử xung quanh (như DNA, protein, lipid, …) gây ra đột biến DNA, biến tính protein và oxi hóa lipid dẫn đến nhiều bệnh nguy hiểm.
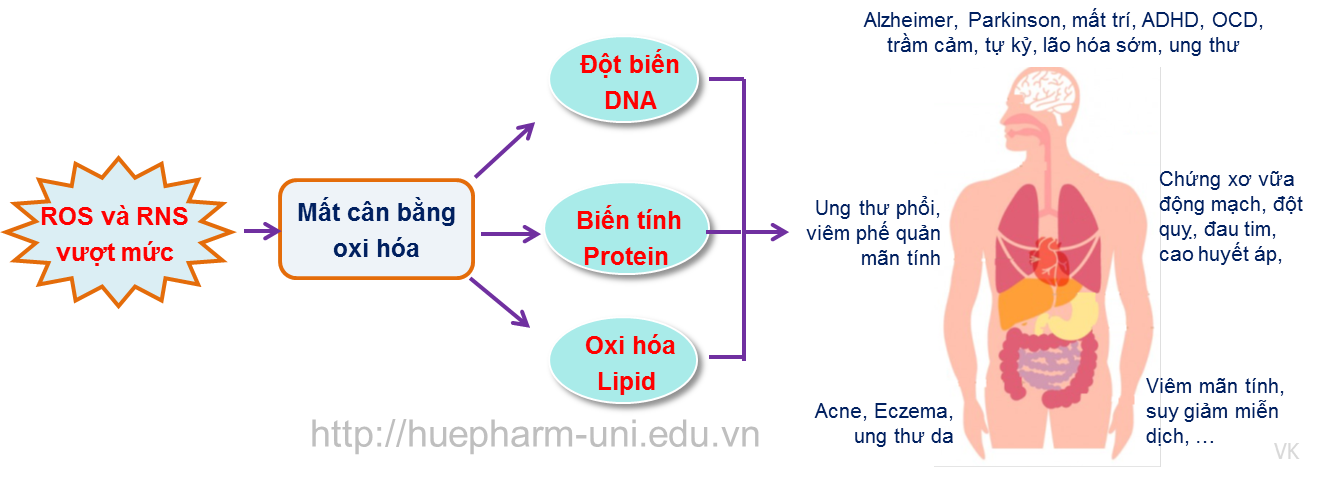
Sự nguy hiểm của mất cân bằng oxi hóa
Ngoài ra, electrophile (chất/gốc có ái lực với điện tử) tồn tại xung quanh ta là tác nhân nguy hiểm từ bên ngoài cho cơ thể. Loại chất/gốc này dễ dàng kết hợp với gốc lưu luỳnh linh động của protein, dẫn đến bất hoạt, biến tính gây rối loạn, độc cho tế bào.
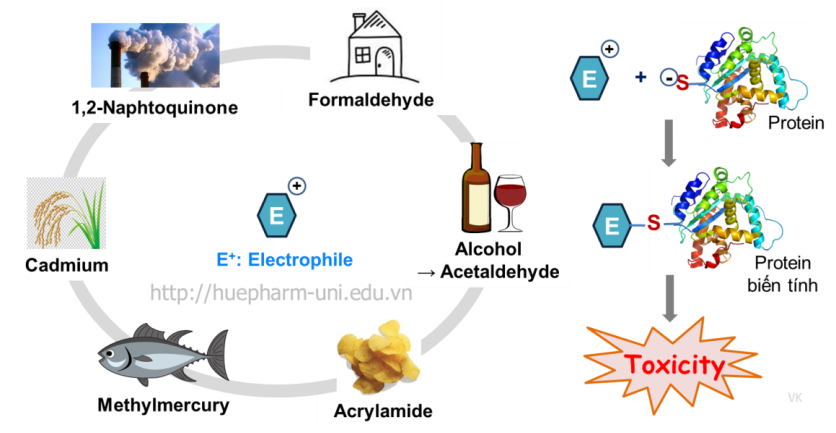
Nguồn và cơ chế gây độc của electrophile
Để bảo vệ, cơ thể tạo ra các chất chống oxi hóa nội sinh: glutathione (GSH), SOD, catalase, peroxidase … Như GSH là một chất chống ôxy hóa quan trọng, có khả năng giúp các thành phần quan trọng của tế bào ngăn ngừa tác hại do các ROS và kim loại nặng gây ra.
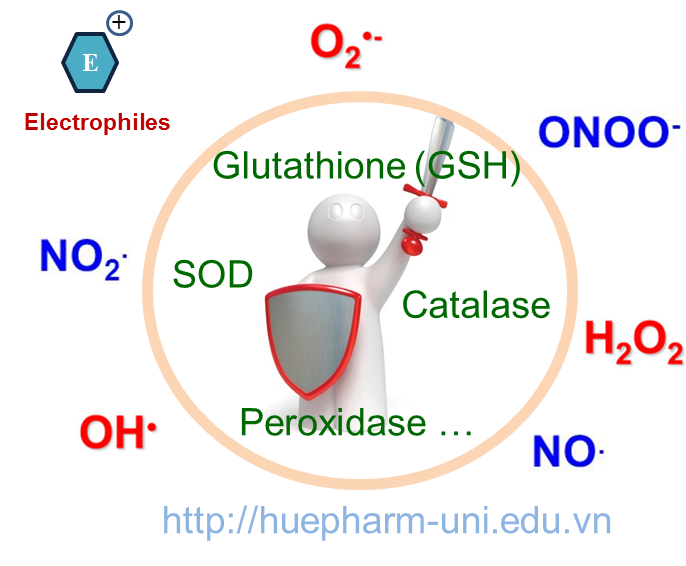
Các chất chống oxi hóa nội sinh
Các công trình nghiên cứu gần đây chỉ ra rằng, các hoạt chất hydropersulfide có khả năng phản ứng với ROS và electrophile mạnh hơn rất nhiều so với các chất chống oxi hóa nội sinh thông thường trên.
Một ví dụ nghiên cứu của Tomoaki Ida và cộng sự cho thấy, trong sự có mặt của enzyme GSR (Glutathione reductase), GSSSG (0,2 mM) được chuyển hóa, tạo ra GSSH ( glutathione hydropersulfide). Hydropersulfide này nhanh chóng khử hoàn toàn H2O2 (0,1 mM) trong khi GSH (0,2 mM) chỉ khử được một lượng nhỏ. Hay theo ước tính, khả năng phản ứng của cysteine hydropersulfide (CysSSH) cao hơn của GSH 1000000 lần.

Khả năng khử H2O2 của các RSS Vai trò bảo vệ của RSSH

Đặc điểm và tính chất của RSH và RSSH giải thích hoạt tính của RSSH mạnh hơn nhiều lần so với RSH.
Pha zero:
Khi các cơ chất từ bên ngoài vào cơ thể sẽ trải qua phản ứng oxy hóa do enzym Cytochrome P450 xúc tác, cơ chất bị ion hóa do các phân tử bị mất điện tử (pha 1), tiếp theo là xảy ra các phản ứng kết hợp giữa ion cơ chất với GSH (pha 2) và thải trừ các chất chuyển hóa phân cực này ra không gian ngoại bào thông qua chất mang protein đa kháng thuốc (MRP) (pha 3). Nhận thấy vai trò bảo vệ RSSH nói riêng và RSS nói chung này, nhóm nghiên cứu của Akaike đề xuất một khái niệm mới rằng có phản ứng pha zero do RSS thực hiện để bắt giữ các electrophile ngay từ ban đầu (trước pha 1) trong quá trình chuyển hóa để giải độc chất.

Quá trình chuyển hóa giải độc chất
(P1.)
Nguyễn Viết Khẩn
Tài liệu tham khảo
- Giles et al., (2017), “The Reactive Sulfur Species Concept: 15 Years On”, Journal/Antioxidants (Basel),6, 10.3390/antiox6020038
- Ida et al., (2014), “Reactive cysteine persulfides and S-polythiolation regulate oxidative stress and redox signaling”, Journal/Proc Natl Acad Sci U S A,111, 7606-7611, 10.1073/pnas.1321232111.
- Millikin et al., (2016), “The chemical biology of protein hydropersulfides: Studies of a possible protective function of biological hydropersulfide generation”, Journal/Free Radic Biol Med,97, 136-147, 10.1016/j.freeradbiomed.2016.05.013
- Park et al., (2015), “Persulfides: current knowledge and challenges in chemistry and chemical biology”, Journal/Mol Biosyst,11, 1775-1785, 10.1039/c5mb00216h
- Saund et al., (2015), “The chemical biology of hydropersulfides (RSSH): Chemical stability, reactivity and redox roles”, Journal/Arch Biochem Biophys,588, 15-24, 10.1016/j.abb.2015.10.016
- TakaakiAkaike, (2014), “Role of reactive sulfur species in detoxification of methylmercury: Phase zero reaction for electrophile trapping and detoxification”, Abstracts/Nitric Oxide 42 99–153.
- Ức chế PCSK9 trong dự phòng tim mạch nguyên phát – Bằng chứng mới từ thử nghiệm VESALIUS-CV
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
- Chế độ ăn Keto có thể đẩy nhanh quá trình lão hóa cơ quan
- Một số điểm mới trong quy định giá dịch vụ khám, chữa bệnh bảo hiểm y tế giữa các bệnh viện cùng hạng trên toàn quốc từ 17/11/2023
