Bệnh tim mạch do xơ vữa mạch máu là nguyên nhân gây tử vong hàng đầu ở bệnh nhân mắc đái tháo đường type 2 và hội chứng chuyển hóa. Bệnh nhân của hội chứng chuyển hóa có các chỉ số huyết áp, đường huyết, các chất béo có hại, chỉ số trọng lượng cơ thể và mỡ bụng vượt quá ngưỡng bình thường, bao gồm. Nguyên nhân của xơ vữa mạch máu trong đái tháo đường type 2 là do sự đề kháng insulin, dẫn đến rối loạn mỡ máu và sản sinh xơ vữa ở thành mạch.
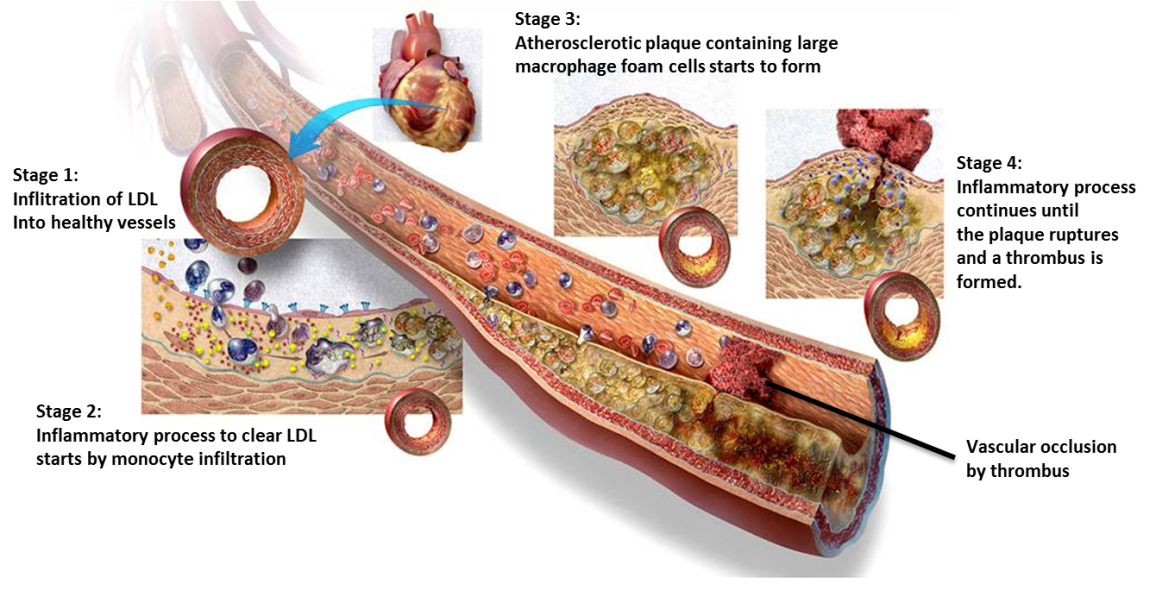
Hình 1. Quá trình hình thành mảng xơ vữa động mạch và vai trò của tế bào xốp
(nguồn http://www.heartnutrition.info/cardiovascular-disease-causes-consequence/)
Nhóm nghiên cứu của đại học Washington, Hoa Kỳ đã tiến hành nghiên cứu trên mô hình chuột với hội chứng chuyển hóa (béo phì, giảm khả năng dung nạp glucose). Trong nghiên cứu này, S597, một phân tử peptide tổng hợp mô phỏng tác dụng insulin, cho thấy khả năng làm giảm đường máu cũng như làm giảm sự tiến triển của các mảng xơ vữa động mạch (khác với insulin, không có khả năng phòng chống xơ vữa động mạch)
Nghiên cứu này được công bố trên tạp chí Diabetes của hiệp hội Đái tháo đường Hoa Kỳ vào tháng 2 năm 2018. Nhóm nghiên cứu gồm các nhà khoa học đến từ Viện nghiên cứu Đái tháo đường của đại học Washington, với người đứng đầu công trình nghiên cứu là Tiến sĩ Jenny Kanter. Nghiên cứu được tiến hành với sự hợp tác của công ty Novo Nordisk.
S597 là một chuỗi acid amin đơn và không hề có cấu trúc như insulin, nhưng nó có thể kích hoạt insulin thụ thể. Tuy nhiên, không giống như insulin, S597 thể hiện tính chọn lọc cao trong các phản ứng của tế bào. Cụ thể, S597 ưu tiên hoạt hóa con đường tín hiệu Akt, liên quan đến chức năng làm hạ đường máu và các lợi ích khác. Bên cạnh đó, nó hoạt hóa con đường tín hiệu Erk ở mức độ yếu hơn, hoặc thậm chí ức chế sự kích hoạt của con đường này, làm hạn chế các tác động không có lợi.
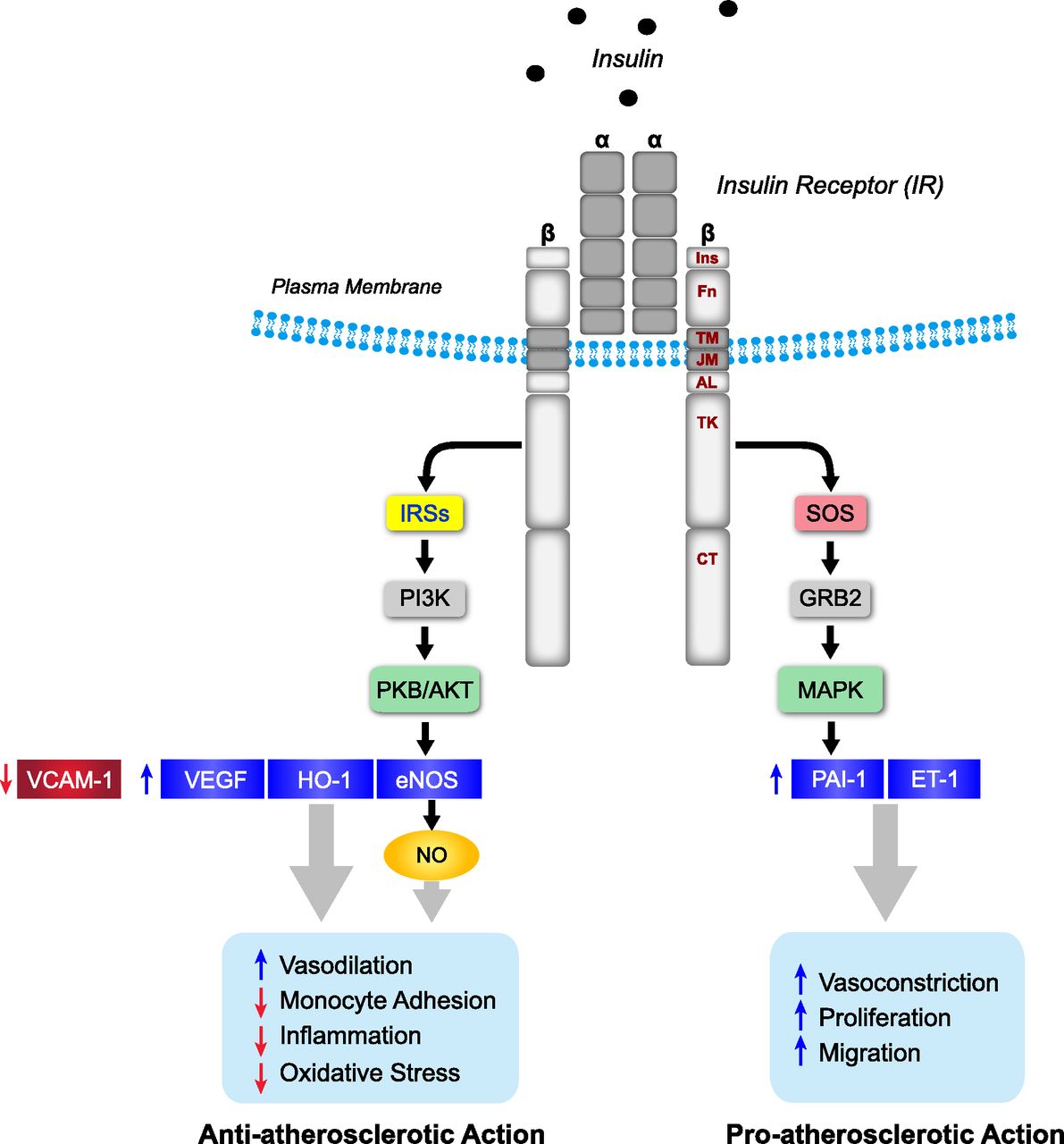
Hình 2. Con đường tín hiệu của insulin: nhánh hoạt hóa Akt (có lợi) và
nhánh hoạt hóa MAPK/ERK (có hại và đóng vai trò trong việc hình thành xơ vữa)
(nguồn King et al., Diabetes 2016, 65(6): 1462-1471)
Điều đáng lưu ý là S597 có thể làm chậm mảng xơ vữa động mạch trên chuột thí nghiệm. Xơ vữa động mạch bắt nguồn từ các mảng chất béo xuất hiện ở thành mạch máu. Khi các mảng chất béo này xuất hiện, chúng kích hoạt quá trình viêm và thu hút các tế bào miễn dịch, làm tăng tốc độ hình thành mảng vữa. Do đó, chứng tăng bạch cầu (leukocytosis) được cho là có vai trò quan trọng trong cơ chế bệnh sinh của bệnh xơ vữa động mạch. Trong số các tế bào miễn dịch, bạch cầu đơn bào và thực bào, là các tác nhân có hại trong việc hình thành mảng xơ vữa. Chúng hấp thu chất béo và trở thành tế bào xốp (foam cells). Các tế bào này kết tụ lại và chết đi, hình thành phần nhân của các mảng vữa. Nếu mảng vữa rơi ra, có thể hình thành cục máu đông ở trong thành mạch tim và não.
Ở trên chuột được tiêm S597, các nhà nghiên cứu nhận thấy lượng tế bào gốc hình thành máu trong tủy xương giảm đi so với chuột khỏe mạnh, đồng nghĩa với việc giảm số lượng bạch cầu đơn bào trong máu do S597 ức chế con đường tín hiệu Erk. Ngoài ra, số lượng thực bào chết ở trong nhân mảng vữa cũng ít hơn ở chuột tiêm S597. Những tác động này lên số lượng bạch cầu đơn bào và thực bào khiến các mảng vữa phát triển chậm hơn. Điều đáng lưu ý là S597 không làm thay đổi hàm lượng cholesterol trong huyết tương cũng như phản ứng viêm hệ thống.
Theo giáo sư Bornfeldt, chủ nhiệm đề tài, “Thuốc hạ cholesterol như statin đang là hướng trị liệu đầu tay cho bệnh xơ vữa động mạch. Chúng tôi hy vọng kết quả của nghiên cứu này sẽ đưa ra một hướng trị liệu mới với vai trò là một phương pháp phòng ngừa bệnh tim mạch do xo vữa liên quan đến hội chứng chuyển hóa và đái tháo đường type 2”.
DS. Trương Thị Thảo Nguyên
Tài liệu tham khảo:
- https://www.sciencedaily.com/releases/2018/02/180226152654.htm
- Kanter, J.E., et al., A Novel Strategy to Prevent Advanced Atherosclerosis and Lower Blood Glucose in a Mouse Model of Metabolic Syndrome. Diabetes, 2018.
- Awiqli (Insulin Icodec): Giải pháp insulin nền mỗi tuần một lần dành cho bệnh nhân đái tháo đường
- Vai trò của dược sĩ trong tiêm chủng người lớn – Thực trạng, rào cản và chiến lược tiếp cận
- Ức chế PCSK9 trong dự phòng tim mạch nguyên phát – Bằng chứng mới từ thử nghiệm VESALIUS-CV
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
