Công nghệ nano là ngành khoa học thực hiện việc nghiên cứu và ứng dụng các vật liệu có kích thước cực nhỏ (10 đến 1000 nm) dựa vào tính chất khác biệt của vật liệu khi ở kích thước này và có thể ứng dụng cho tất cả các lĩnh vực khác nhau như vật lý, hóa học, sinh học, y học,… Tổ chức khoa học châu Âu (European Science Foundation) mở rộng khái niệm nano trong y học cho các tiểu phân có kích thước đến hàng trăm nanomét, khái niệm này phù hợp hơn với định nghĩa của tiểu phân nano dùng để đưa thuốc đến nơi tác dụng.
Công nghệ nano dược hình thành trên cơ sở áp dụng thành tựu của công nghệ nano nói chung vào lĩnh vực nghiên cứu chế tạo các tiểu phân nano dược phẩm, các hệ mang thuốc nano hoặc các thiết bị nano dùng trong chẩn đoán và điều trị bệnh.
Trong ngành dược, việc sử dụng các hệ thống mang thuốc ở kích thước nano có thể đem đến một liệu pháp điều trị khả thi nhờ vào tính đặc hiệu hoặc tác dụng tại đích kết hợp với việc giải phóng thuốc tối ưu, từ đó giúp tăng cường tác dụng dược lý đồng thời giảm tác dụng phụ có hại của thuốc.
Các dược phẩm nano (nanopharmaceuticals) được định nghĩa là các phức hợp có kích thước nano, đơn giản như là các tiểu phân nano, nhũ tương nano, phức hợp polyme, hoặc phức tạp hơn như các hệ đa thành phần kích thước nano có chứa thuốc, protein hoặc gen, các phối tử hướng đích và các tín hiệu để có thể phát hiện trên thử nghiệm in vitro hoặc in vivo.
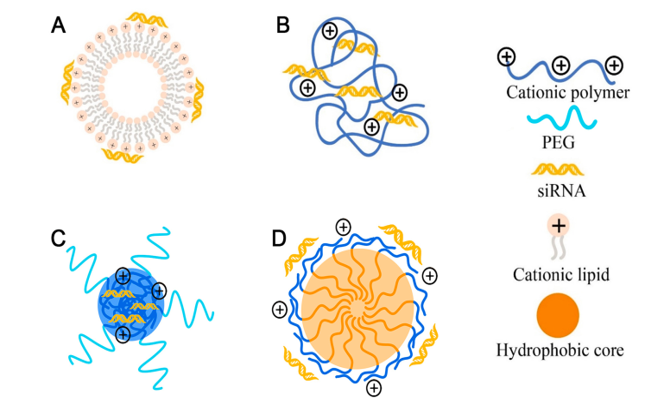
Về phân loại, có rất nhiều dạng thuốc chứa tinh thể nano hoặc hệ mang thuốc nano. Trong hệ mang thuốc nano, dược chất được bao gói trong các chất mang như dendrime, liposome, nano polyme, nano lipid, nano lai lipid-polyme/polyme-lipid.
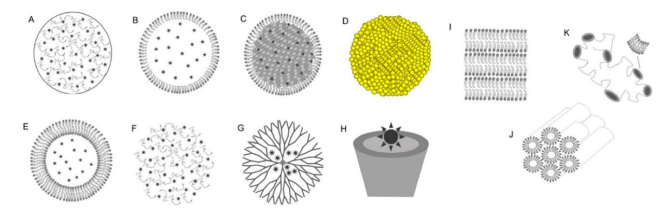
Các loại nano khác nhau sử dụng trong vận chuyển thuốc: A. Nano polymer; B.Hệ mang thuốc có cấu trúc lipid (NLC); C.Nano lipid rắn (SLN); D. Nano kim loại; E.Liposome; F. Nanohydrogel; G. Dendrime; H. Cyclodextrin; và hệ tinh thể lỏng (liquid crystalline system) ở: I. Dạng xếp tầng; J. Dạng lục giác; K. Dạng cubic.
Hệ mang thuốc nano thường có nhiều ưu điểm như khả năng vận chuyển thuốc đặc hiệu, độ ổn định cao, khả năng thấm qua màng sinh học cao, sinh khả dụng được tăng cường, và tác dụng kéo dài. Bằng cách thay đổi các đặc tính sinh dược học của các chất tiềm năng dùng làm thuốc mới, việc bào chế các dạng thuốc chứa hệ mang thuốc nano có thể là một giải pháp hứa hẹn để giữ vững các đặc tính của thuốc. Các đặc tính lý hóa của các tiểu phân nano như kích thước tiểu phân, điện thế bề mặt và khả năng thân dầu sẽ ảnh hưởng đến đặc tính hấp thu qua màng sinh học của chúng. Các tiểu phân nano có kích thước nhỏ thường có khả năng hấp thu thông qua các nang của biểu mô cao hơn so với các tiểu phân có kích thước lớn. Các tiểu phân nano có thể đi vào tế bào thông qua quá trình nội thực bào như nhập bào qua trung gian caveola và clathrin, ẩm bào. Ngược lại, các tiểu phân lớn hơn có thể bị opsonin hóa nhanh (các protein có khả năng bám dính vào vật ngoại lai hay tế bào giúp chúng dễ bị nhận diện bởi quá trình thực bào) và loại khỏi hệ tuần hoàn thông qua các đại thực bào của hệ lưới nội mô.
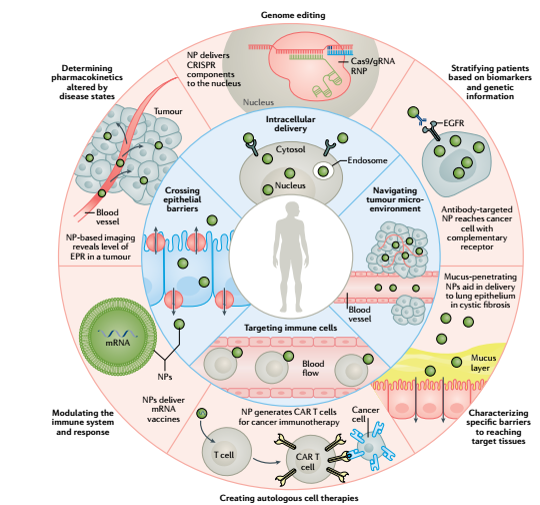
Các rào cản sinh học cần vượt qua nhằm ứng dụng công nghệ nano trong lĩnh vực Y-Dược
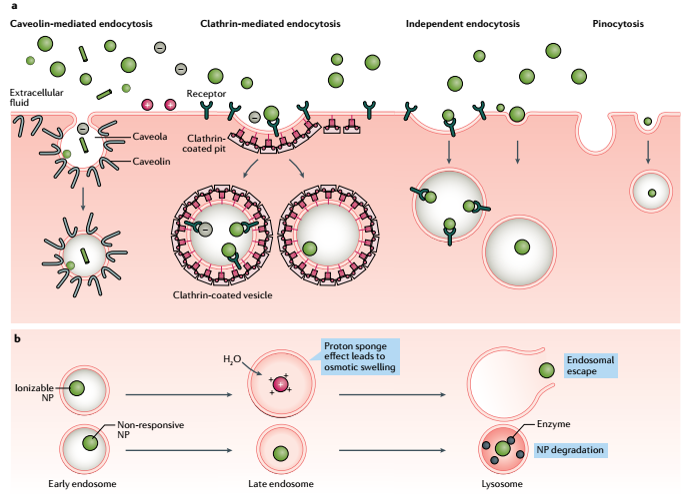
Các con đường nhập bào chung và số phận của tiểu phân nano trong tế bào: a. Các con đường nhập bào; b. TP nano sau khi đi vào tế bào
Trong việc thiết kế công thức của tiểu phân nano, cần thiết làm giảm thiểu khả năng opsonin hóa và kéo dài thời gian tuần hoàn của các tiểu phân nano. Điều này có thể đạt được bằng cách bao bề mặt của tiểu phân nano bằng các polyme hoặc chất diện hoạt thân nước và/hoặc thiết kế công thức tiểu phân nano với các đồng polyme phân hủy sinh học có thêm các phần thân nước như polyethylen glycol, poloxame, poloxamin và polysorbat.
Các tiểu phân nano có điện thế bề mặt dương có thể tương tác với điện thế âm của mucin do chứa các hợp phần acid sialic và đường, dẫn đến việc tăng cường quá trình vận chuyển qua màng tế bào và quá trình nội bào nhờ các tế bào biểu mô.
Việc “chức năng hóa” bề mặt tiểu phân nano với các chất tăng cường tính thấm qua màng hoặc các phức hợp có khả năng gắn kết với các thụ thể trên màng tế bào có thể thúc đẩy khả năng vận chuyển qua màng tế bào của các thuốc được bao gói. Ngoài khả năng vận chuyển qua màng tế bào, các thuốc kích thước nano được bao gói hay liên kết với các polyme bám dính sinh học hoặc các chất tạo phức chelat có thể giúp tăng cường khả năng vận chuyển liên bào của các thuốc thông qua việc điều hòa các khe hở hẹp giữa các tế bào. Việc cải biến bề mặt (surface modification) của các tiểu phân nano với các protein đặc hiệu, các kháng thể và các phân tử sinh học khác có thể được sử dụng để thiết kế các thuốc có tác dụng chọn lọc trên các mô cụ thể. Ngoài ra, cũng có thể sử dụng các thành phần trong công thức có khả năng nhạy cảm với các tín hiệu vi môi trường bên trong (như nhạy cảm với pH, nhạy cảm với enzym) hay các tín hiệu ngoại cảnh (như từ trường, ánh sáng). Các giải pháp này giúp tăng cường khả năng chẩn đoán và trị liệu, đồng thời, giảm tác dụng không mong muốn của các thuốc điều trị có cửa sổ điều trị hẹp.
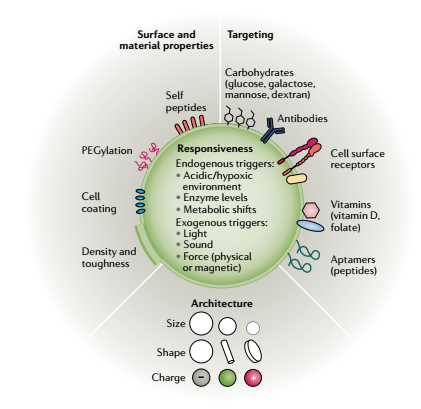
Các đặc tính bề mặt của tiểu phân nano giúp tăng cường khả năng đưa thuốc
Công nghệ nano trong điều trị bệnh
Kể từ khi liposome được mô tả lần đầu tiên vào những năm 1960 và được đề xuất làm hệ vận chuyển thuốc trong điều trị bệnh, công nghệ nano đã có tác động đáng kể đến sự phát triển của các hệ vận chuyển thuốc. Rất nhiều các vật liệu và thiết bị nano hữu cơ, vô cơ khác nhau đã được sử dụng làm các hệ vận chuyển để phát triển các phương thức điều trị hiệu quả. Cho đến nay, đã có hơn 24 sản phẩm điều trị dựa trên công nghệ nano được FDA chấp nhận dùng trên lâm sàng và nhiều sản phẩm khác vẫn đang trong quá trình thử nghiệm lâm sàng trong đó phần lớn là các sản phẩm thuộc thế hệ 1 – thế hệ gồm các hệ vận chuyển không hướng đích (như liposome và các nano polyme).
Gần đây, nhiều nhà nghiên cứu đã và đang tập trung vào lĩnh vực nano trong Y-Dược và những tiến bộ của nó trong chẩn đoán và điều trị nhiều bệnh khác nhau như ung thư, COVID 19, bệnh lý nội tiết như đái tháo đường,… Trong phạm vi bài tổng quan này, chỉ tập trung chính giới thiệu đôi nét về tình hình ứng dụng công nghệ nano trong chẩn đoán và điều trị bệnh ung thư và COVID-19 cho đến nay.
Điều trị bệnh ung thư
Cùng với sự phát triển của các ngành khoa học khác, trong vài thập kỷ qua, ngành Dược trên thế giới đã vận dụng những thành quả của khoa học nano nói chung vào lĩnh vực nghiên cứu phát triển các dạng thuốc mới, từ đó tạo ra cuộc cách mạng cho ra đời các hệ phân phối thuốc mới nhằm khắc phục những hạn chế của các dược chất và dạng thuốc truyền thống trong điều trị các bệnh hiểm nghèo như ung thư, HIV, bệnh về gen,…. Ứng dụng công nghệ nano để điều trị bệnh ung thư là một bước tiến trong ngành dược, do việc tăng sinh khả dụng và đưa thuốc tới đích.
Bệnh ung thư vẫn là một thách thức của y học hiện nay. Bất chấp những nỗ lực và nhiều tiến bộ trong suốt 30 năm qua, việc kiểm soát bệnh ung thư vẫn còn những hạn chế. Các hóa chất mới thường bị hạn chế sử dụng do độc tính cao hoặc do hiệu quả thấp. Do vậy, việc tăng nồng độ thuốc tại tế bào ung thư và quá trình phân phối thuốc sẽ tiếp tục đóng vai trò quan trọng trong việc tạo ra những tác nhân an toàn và hiệu quả. Việc phân phối thuốc có thể được điều chỉnh bằng cách thay đổi đường sử dụng hoặc thay đổi thiết kế công thức thuốc.
Trong công nghệ dược phẩm, công nghệ nano đã được ứng dụng để làm tăng khả năng hấp thu của thuốc qua đó làm tăng hiệu quả điều trị. Các tiểu phân nano có thể giải phóng thuốc tại đích tác dụng với liều lượng và khoảng thời gian như dự kiến, đặc biệt với các tế bào khối u, kết quả là làm tăng hiệu quả điều trị và giảm thiểu độc tính cho cơ thể người bệnh.
Việc thiết kế hệ mang thuốc nano thường được dựa trên các đặc điểm sinh học của khối u. Ba đặc điểm sinh học của khối u được sử dụng làm căn cứ cho việc thiết kế tiểu phân nano chứa các thuốc chống ung thư định hướng đến các khối u đích, bao gồm:
– Cấu trúc bất thường của lớp lót nội mạc của các mạch máu đi qua khối u dẫn đến hiệu ứng tăng tính thấm và lưu giữ (EPR – enhanced permeability and retention).
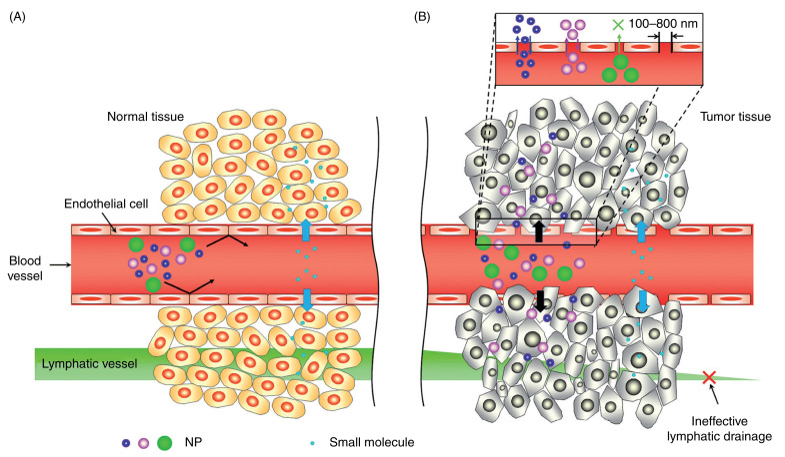
Hiệu ứng tăng tính thấm và lưu giữ
– Vi môi trường khác biệt ở khối u như: pH ngoại bào của khối u thấp hơn cho phép phân phối thuốc từ các tiểu phân nano tại pH thấp hoặc định hướng các khối u đích của các thuốc có nhạy cảm với acid; thân nhiệt cao cục bộ,…
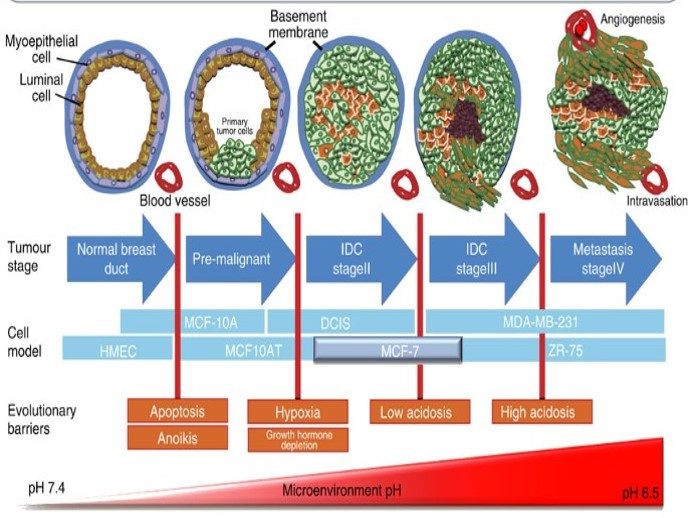
pH ngoại bào của khối u
– Các kháng nguyên đặc hiệu của khối u giúp định hướng các tiểu phân nano thuốc đến các tế bào khối u có bộc lộ các kháng nguyên này.
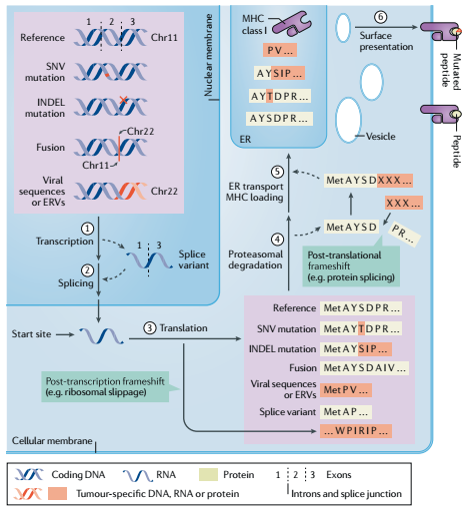
Quá trình bộc lộ kháng nguyên đặc hiệu ở khối u
Ngoài ra, hệ mang thuốc nano có ưu điểm hơn dạng thuốc tự do thông qua quá trình ức chế lại sự đề kháng thuốc của các tế bào ung thư. Mặc dù các thuốc có khả năng ức chế bơm ngược để hạn chế khả năng đề kháng thuốc đã được phát triển, tuy nhiên vẫn còn những hạn chế nhất định. Do đó, các tiểu phân nano đã được thiết kế nhằm sử dụng hiệu ứng EPR để thoát khỏi thành mạch máu của khối u, để hướng đích các thụ thể trên bề mặt của các tế bào khối u và để đi vào tế bào khối u thông qua quá trình nội thực bào trước khi giải phóng thuốc bên trong. Phương pháp này cho phép đưa một nồng độ thuốc cao trong nội bào giúp vượt qua sự đề kháng thuốc thông qua quá trình bơm ngược của các P-glycoprotein của tế bào khối u.
Về cơ chế tác dụng, các tiểu phân nano gây ra quá trình tự chết tế bào đối với các tế bào ung thư thông qua hàng loạt cơ chế, trong đó, quá trình tự chết tế bào trung gian qua các gốc tự do được nghiên cứu nhiều nhất. Ngoài ra, quá trình điều hòa tăng hay giảm các protein, ngăn ngừa các yếu tố miễn dịch, ức chế sự phiên mã, tác dụng gây độc tế bào tại vị trí đích,… là các cơ chế khác gây ra quá trình tự chết tế bào đối với tế bào ung thư.
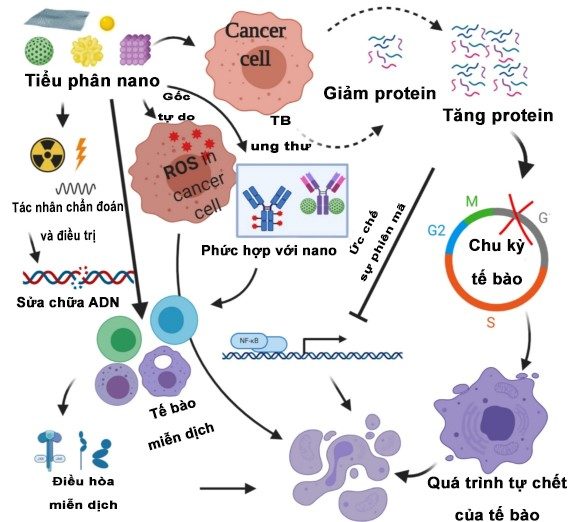
Các cơ chế tự chết của tế bào ung thư do tác động của tiểu phân nano
Một số chế phẩm nano sử dụng trong điều trị bệnh ung thư
|
Chế phẩm |
Dược chất/Hàm lượng/Dạng nano |
Nhà sản xuất |
Chỉ định |
|
Abraxane |
Paclitaxel gắn albumin/100mg/Nano polyme |
Abraxis BioScience, LLC, Tập đoàn Celgene, Mỹ |
Ung thư tuyến tụy, ung thư vú di căn, ung thư phổi không tế bào nhỏ |
|
Oncaspar |
Phức hợp L-asparaginase gắn với PEG |
Enzon Pharmaceuticals, Mỹ
|
Ung thư các mô tạo máu |
|
DaunoXome |
Daunorubicin citrat/50mg/Liposome |
Gilead Science, Mỹ |
Ung thư mô liên kết ở bệnh nhân AIDS |
|
DepoCyt |
Cytarabin/50mg/ Liposome |
Almac Pharma Services Ltd, Craigavon, Anh |
Viêm màng não ở bệnh bạch cầu |
|
Doxil/Caelyx |
Doxorubicin HCl /20mg/10 ml hoặc 50mg/25ml/Liposome PEG hóa |
Alza/Janssen, Tập đoàn Johnson Johnson, Mỹ |
Ung thư tử cung, ung thư vú, ung thư mô liên kết do AIDS, đa u tủy |
|
Genexol-PM |
Paclitaxel/30-100mg/micell polyme PEG-PLA |
Samyang, Hàn Quốc |
Ung thư vú, ung thư phổi, ung thư tử cung |
|
Mepact |
Mifamurtid/4mg/ Liposome |
Takeda Italia Farmaceutici SpA, Cerano, Ý |
Ung thư xương không di căn |
|
Myocet |
Doxorubicin HCl/50mg/Liposome |
Sopherion Therapeutics, Mỹ |
Ung thư vú di căn |
|
Onivyde |
Irinotecan/43mg/10ml/ Liposome PEG hóa |
Merrimack, Mỹ |
Ung thư tụy di căn |
|
Vyxeos |
Daunorubicin+Cytarabin/44+100mg/Liposome |
Jazz Pharma, Cộng hòa Ireland |
Ung thư bạch cầu dòng tủy cấp tính |
|
Zolsketil pegylated liposomal |
Doxorubicin HCl/Liposome PEG hóa |
Accord Healthcare Polska (Ba Lan) & Accord Healthcare B.V.(Hà Lan) |
Ung thư vú và buồng trứng, ung thư mô liên kết do AIDS, đa u tủy |
|
Hensify (NBTXR3) |
Nano Hafnium oxid |
Nanobiotix, Pháp |
Ung thư mô mềm |
|
NanoTherm |
Nano oxid sắt |
Magforce Nanotechnologies (Đức) |
U não |
Hệ mang thuốc nano thường có nhiều ưu điểm như khả năng vận chuyển thuốc đặc hiệu, độ ổn định cao, khả năng thấm qua màng sinh học cao, sinh khả dụng được tăng cường, và tác dụng kéo dài, giảm tác dụng không mong muốn của thuốc. Bằng cách thay đổi các đặc tính sinh dược học của các chất tiềm năng dùng làm thuốc mới, việc bào chế các dạng thuốc chứa hệ mang thuốc nano có thể là một giải pháp hứa hẹn để giữ vững các đặc tính của thuốc. Các đặc tính lý hóa của các tiểu phân nano như kích thước tiểu phân, điện thế bề mặt và khả năng thân dầu sẽ ảnh hưởng đến đặc tính hấp thu qua màng sinh học của chúng. Các tiểu phân nano có kích thước nhỏ thường có khả năng hấp thu thông qua các nang của biểu mô cao hơn so với các tiểu phân có kích thước lớn. Các tiểu phân nano có thể đi vào tế bào thông qua quá trình nội thực bào như nhập bào qua trung gian caveola và clathrin, ẩm bào. Ngược lại, các tiểu phân lớn hơn có thể bị opsonin hóa nhanh (là các protein có khả năng bám dính vào vật ngoại lai hay tế bào giúp chúng dễ bị nhận diện bởi quá trình thực bào) và loại khỏi hệ tuần hoàn thông qua các đại thực bào của hệ lưới nội mô.
Trong việc thiết kế công thức của tiểu phân nano, cần thiết làm giảm thiểu khả năng opsonin hóa và kéo dài thời gian tuần hoàn của các tiểu phân nano. Điều này có thể đạt được bằng cách bao bề mặt của tiểu phân nano bằng các polyme hoặc chất diện hoạt thân nước và/hoặc thiết kế công thức tiểu phân nano với các đồng polyme phân hủy sinh học có thêm các phần thân nước như polyethylen glycol (PEG), poloxame, poloxamin và polysorbat.
Ví dụ như trong công thức Zolsketil vừa được chấp thuận vào tháng 5/2022 ở Châu Âu (bảng 1), việc sử dụng liposome được PEG hóa đã làm chậm lại quá trình đào thải của thuốc, cho phép thuốc có thể tuần hoàn lâu hơn ở trong máu. Liposome Zolsketil chứa doxorubicin có kích thước trung bình khoảng 100 nm nên có thể đi qua được các “lỗ rò” ở các mao mạch bị bất thường quanh khối u. Do vậy, doxorubicin dạng liposome được PEG hóa có thể tích phân bố khu trú hơn và tốc độ đào thải chậm hơn (phụ thuộc vào chất tạo hệ liposome) so với doxorubicin truyền thống. Ở cùng một mức liều, nồng độ thuốc trong huyết tương và giá trị AUC (diện tích dưới đường cong) của doxorubicin dạng liposome PEG hóa cao hơn đáng kể so với các giá trị này của các dạng bào chế chứa doxorubicin truyền thống.
Điều trị COVID-19
Sự bùng phát của dịch bệnh do virus corona năm 2019 đã đe dọa an toàn sức khỏe toàn cầu với triệu chứng nhiễm trùng đường hô hấp cấp tính, tỉ lệ mắc và tử vong cao.
Chiến lược sử dụng công nghệ nano chống lại virus SARS-CoV-2 liên quan đến cơ chế có thể ảnh hưởng đến quá trình đi vào tế bào chủ của virus. Cho đến nay, mục tiêu ưu tiên để kiểm soát nhanh sự bùng phát virus là tiêm vaccin. Việc đưa vaccin bằng hệ nano có thể tăng cường hiệu quả và sự tạo miễn dịch của vaccin bằng cách bảo vệ kháng nguyên khỏi phân hủy, giải phóng kiểm soát và kéo dài cũng như kiểm soát quá trình nội bào và thực bào.
Các vaccin phòng ngừa virus Covid 19 sử dụng công nghệ nano
|
Dạng nano |
Thành phần kháng nguyên |
Vai trò và kết quả |
|
Nano lipid |
Vaccin mARN – Moderna (Mỹ) |
Chất mang mARN hiệu quả/an toàn in vivo |
|
Vaccin mARN – BioNTech/Pfizer (Mỹ) |
Chất mang mARN hiệu quả/an toàn in vivo |
|
|
Vaccin mARN (pha I/II) – Arctutus Therapeutics Ltd |
Chất mang mARN hiệu quả/an toàn in vivo |
|
|
Vaccin mARN (pha III) – CureVac AG (Đức) |
Chất mang mARN hiệu quả/an toàn in vivo |
|
|
Nano lipid thế hệ mới |
Vaccin mARN (pha I) Đại học Chunglalongkorn (Thái Lan) |
Chất mang mARN hiệu quả/an toàn in vivo |
|
Tiểu phân nano giống virus |
Vaccin tiểu đơn vị (kết hợp hệ tăng cường Matrix-M) – Novavax (Mỹ) |
Ổn định nhiệt, ái lực cao với thụ thể ACE2, trung hòa đáng kể virus |
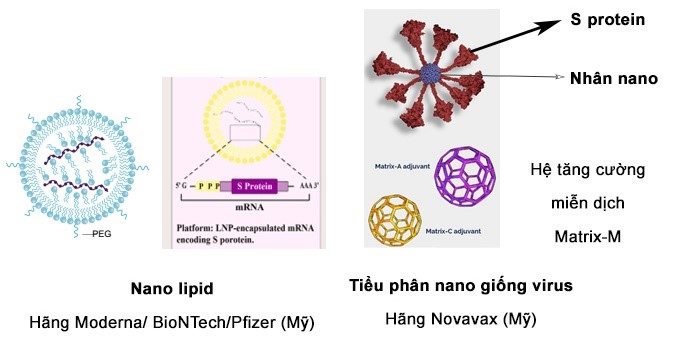
Minh họa cấu trúc của các vaccin phòng ngừa virus COVID-19 sử dụng công nghệ nano
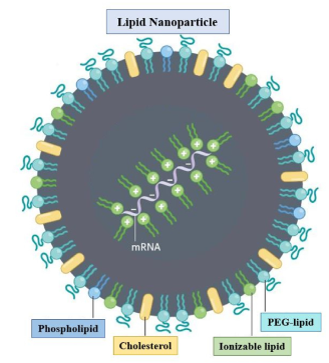
Cấu trúc của tiểu phân nano lipid mang mARN
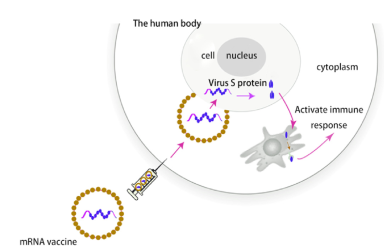
Cơ chế gây đáp ứng miễn dịch của vaccine mARN
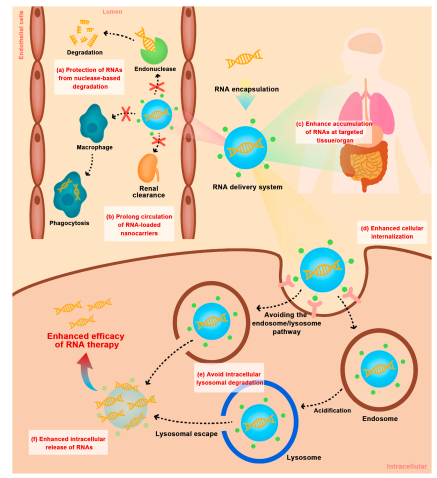
Các rào cản sinh học nội và ngoại bào trong vận chuyển các RNA sử dụng các giá mang không phải virus
Cơ chế bảo vệ RNA khỏi sự phân hủy của nuclease bằng sự bao gói

Cơ chế bảo vệ RNA khỏi sự phân hủy của nuclease bằng sự hấp phụ tĩnh điện
Công nghệ nano trong chẩn đoán bệnh
Công nghệ nano còn được sử dụng trong thiết kế các cảm biến sinh học để có thể phát hiện nhanh và cùng một lúc nhiều chất chỉ điểm sinh học (biomarker) của các bệnh lý với độ nhạy cao và lượng mẫu nhỏ. Sự ra đời của cảm biến sinh học, ống nano carbon, thiết bị nano bằng polyme, và các chip sinh học với độ tin cậy và độ nhạy cao giúp phát hiện sớm các bệnh lý nguy hiểm đến tính mạng như ung thư, tim mạch,… ngoài ra, hệ thống lab-on-chip chứa các vật liệu cảm biến mới hoặc các cảm biến dựa trên chip sinh học cũng đã và đang được phát triển nhằm đem đến hiệu quả tốt hơn trong chẩn đoán và điều trị bệnh tật.
Đồng thời, công nghệ nano còn có vai trò trong chẩn đoán hình ảnh với việc cung cấp một giải pháp nhanh, ít xâm lấn, chính xác hơn để chẩn đoán bệnh ở các giai đoạn sớm cũng như giám sát tiến trình của bệnh. Các tiểu phân nano có thể được kết hợp hoặc đánh dấu bằng các phân tử nhỏ, hoặc các ion phức, kim loại hoặc các nano tinh thể để có thể được phát hiện bằng các thiết bị chẩn đoán hình ảnh như máy chụp cộng hưởng từ (MRI – magnetic resonance imaging), chụp X-quang (X-ray imaging) và chụp vi tính cắt lớp (CT – computed tomography imaging), chụp xạ hình cắt lớp positron (PET – positron emission tomography imaging), chụp cắt lớp đơn photon (SPECT – single photon emission computed tomography imaging), hoặc các kỹ thuật kết hợp PET/CT, SPECT/CT. Ví dụ: các tiểu phân nano vàng, chấm lượng tử (quantum dot), tiểu phân nano oxyd sắt từ, phức hợp của gadolinium. Trong đó, các tính chất như kích thước, đặc tính bề mặt là các tiêu chí chính ảnh hưởng đến khả năng phân bố, thải trừ, hoặc nhận diện bởi đại thực bào của các tiểu phân nano. Ngoài ra, công nghệ nano còn được ứng dụng để bào chế tiểu phân nano chứa đồng thời tác nhân có tác dụng điều trị và tác nhân có tác dụng chẩn đoán (theranostic nanoparticles).
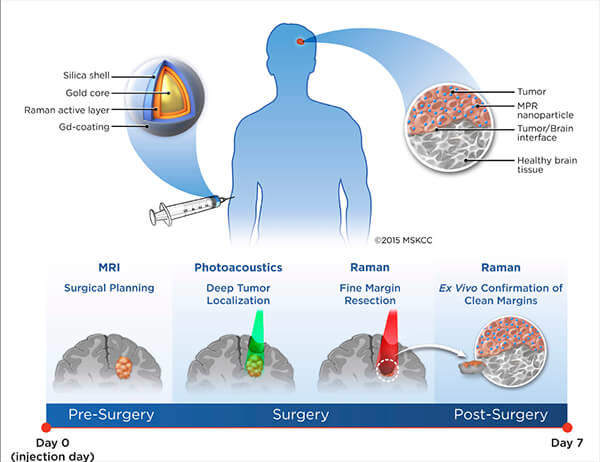
Nguyên lý của tiểu phân nano ứng dụng ba phương thức chẩn đoán hình ảnh là MRI-quang âm-Raman ứng dụng trong lâm sàng
Các tiểu phân nano sử dụng trong chẩn đoán bệnh
|
Dạng nano |
Tác nhân |
Thiết bị |
Hãng sản xuất |
|
Hệ keo sulfur |
99mTc |
SPECT |
Technecoll (Mỹ) |
|
Hệ keo albumin |
99mTc |
SPECT |
Nanocoll (Châu Âu) |
|
Hệ keo SnF2 |
99mTc |
SPECT |
Hepatate (Pháp) |
|
Hệ keo Re2S7 |
99mTc |
SPECT |
Nanocis (Châu Âu) |
|
Oxid sắt bao bởi dextran |
Fe3O4 |
MRI |
Feridex (Mỹ), |
|
Oxid sắt bao bởi carboxydextran |
γ-Fe2O3 |
MRI |
Resovist (Mỹ, Châu Âu), |
|
Oxid sắt bao bởi polyglucose sorbitol carboxymethylether |
γ-Fe2O3 |
MRI |
Faraheme (Mỹ) |
Trong chẩn đoán mắc bệnh, tiểu phân nano vàng, nano silica cũng đã được nghiên cứu để ứng dụng trong chẩn đoán các chất chỉ dấu sinh học (biomarker) trong các bệnh lý do covid 19, ung thư.
Ngoài ra, hiện nay, các công cụ chẩn đoán đã được sử dụng để tầm soát, phát hiện bệnh cũng như để định hướng cho các quy trình mổ hở hoặc xâm lấn tối thiểu nhất. Trong tương lai, với việc phát triển của công nghệ nano, các thiết bị/đầu dò trong chẩn đoán hình ảnh sẽ phát triển để giúp việc chuẩn đoán được thuận lợi hơn cũng như hỗ trợ các bác sĩ, phẫu thuật viên thêm nhiều dữ liệu về cấu trúc, chức năng, dữ liệu ở mức độ phân tử để có chiến lược trị liệu phù hợp với từng cá thể.
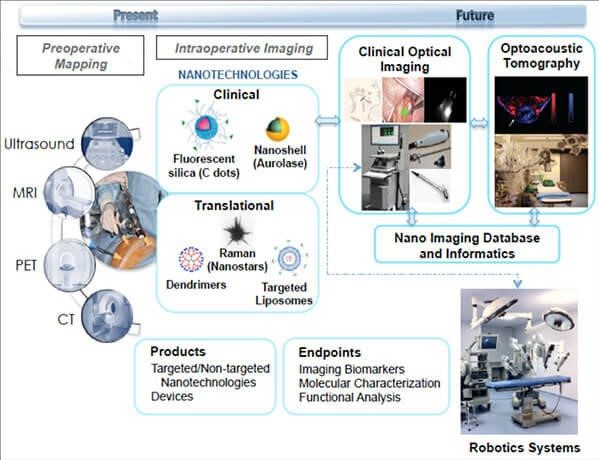
Mô phỏng hiện tại và tương lai của phòng mổ có hỗ trợ bằng hình ảnh ứng dụng công nghệ nano
Mặc dù đã có những thành công trong việc ứng dụng công nghệ nano trong chẩn đoán và điều trị bệnh, cho đến nay, vẫn còn một số rất hạn chế các công thức nano đã bước vào giai đoạn thử nghiệm lâm sàng. Điều này có thể là do các công thức nano phải đối mặt với các vấn đề về độ ổn định, khó mở rộng quy mô và chi phí phát triển của chúng cao hơn nhiều so với các phương pháp điều trị truyền thống, do đó làm cho chúng kém hấp dẫn hơn đối với các ngành công nghiệp dược phẩm. Hơn nữa, việc thiếu các quy trình chuẩn hóa để đánh giá tiền lâm sàng của các công thức liên quan đến mô hình động vật, các chủng loại, đối chứng dương, thời gian điều trị và theo dõi, cản trở việc tạo ra kết quả đồng nhất, mạnh và có thể so sánh được. Điều này, kết hợp với các vấn đề đạo đức và quy định liên quan đến công nghệ nano, cũng như mối quan hệ đối tác hạn chế trong ngành học thuật và cơ sở thử nghiệm không đầy đủ, đã cản trở việc đưa vào lâm sàng của các công thức tiềm năng.
Theo đó, cần tiếp tục việc thiết kế hợp lý các công thức nano an toàn, ổn định và hiệu quả để vận chuyển thuốc/vaccin, có tính đến yêu cầu về một quy trình sản xuất đơn giản, tốt và tiết kiệm chi phí, có thể dễ dàng mở rộng quy mô. Thiết kế và phát triển công thức nano nên tận dụng tiến bộ trong tin sinh học và sàng lọc thông lượng cao liên quan đến sự hiểu biết tốt hơn về các chức năng của protein và lựa chọn các biểu mô ưu thế, lựa chọn các tá dược trong công thức thích hợp. Hơn nữa, những tiến bộ trong phân tích dữ liệu lớn nên được khai thác để trích xuất thông tin từ các dữ liệu thử nghiệm sẵn có. Về mặt này, việc phát triển công thức nano cần dựa trên sự hợp tác của các nhà khoa học dược phẩm, nhà hóa học, kỹ sư, nhà sinh học, nhà tiêm chủng, tin sinh học, v.v.
Các chiến lược phát triển vaccin và hệ trị liệu dựa trên các chất mang nano đã được phát triển trong thập kỷ qua để chẩn đoán, điều trị và phòng ngừa bệnh. Các xét nghiệm sinh học mới dựa trên công nghệ nano đã ra đời giúp tăng độ nhạy, độ đặc hiệu và khả năng tái lặp. Ngoài ra, các chất mang nano khác nhau đã cho thấy kết quả đầy hứa hẹn trên mô hình in vivo, cả trong các phác đồ điều trị và dự phòng. Hy vọng trong tương lai, cùng với sự phát triển của ngành công nghệ nano nói chung thì ứng dụng của nó trong lĩnh vực Y-Dược nhằm chẩn đoán và điều trị bệnh sẽ tạo ra thêm nhiều chế phẩm hữu ích trên thị trường.
Tổng hợp
TS. Hồ Hoàng Nhân
Tài liệu tham khảo:
- Hồ Hoàng Nhân (2022), Công nghệ nano và ứng dụng trong chẩn đoán và điều trị bệnh, Tạp chí Y Dược học (Trường Đại học Y Dược, ĐHH).
- Alasvand N., Urbanska A. M., Rahmati M., Saeidifar M., Gungor-Ozkerim P. S., Sefat F., Rajadas J. & Mozafari M. (2017). Therapeutic Nanoparticles for Targeted Delivery of Anticancer Drugs. 10.1016/b978-0-323-52725-5.00013-7: 245-259.
- Alexis F, Pridgen E, Molnar LK, Farokhzad OC. Factors affecting the clearance and biodistribution of polymeric nanoparticles. Mol Pharm. 2008;5(4):505-15.
- Autio KA, Dreicer R, Anderson J, Garcia JA, Alva A, Hart LL, et al. Safety and Efficacy of BIND-014, a Docetaxel Nanoparticle Targeting Prostate-Specific Membrane Antigen for Patients With Metastatic Castration-Resistant Prostate Cancer: A Phase 2 Clinical Trial. JAMA oncology. 2018.
- Bobo D, Robinson KJ, Islam J, Thurecht KJ, Corrie SR. Nanoparticle-Based Medicines: A Review of FDA-Approved Materials and Clinical Trials to Date. Pharm Res. 2016;33(10):2373-87.
- Centerwatch. FDA Approved Drugs for Oncology 2018 [cited 2018 July]. Available from: https://www.centerwatch.com/drug-information/fda-approved-drugs/therapeutic-area/12/oncology.
- Chen H, Khemtong C, Yang X, Chang X, Gao J. Nanonization strategies for poorly water-soluble drugs. Drug discovery today. 2011;16(7-8):354-60.
- Cornier J, Owen A, Kwade A, Van de Voorde M. Pharmaceutical Nanotechnology, 2 Volumes: Innovation and Production: Wiley; 2017.
- Duran N, Marcato P, Teixeira Z, Duran M, Costa F, Brocchi M. State of the Art of Nanobiotechnology Applications in Neglected Diseases. Curr Nanosci. 2009;5(4):396-408.
- Grabnar PA, Kristl J. The manufacturing techniques of drug-loaded polymeric nanoparticles from preformed polymers. J Microencapsul. 2011;28(4):323-35.
- European Medicines Agency. Zolsketil pegylated liposomal,INN doxorubicin hydrochloride 2022 [7/2022]. Available from: https://www.ema.europa.eu/en/documents/product-information/zolsketil-pegylated-liposomal-epar-product-information_en.pdf.
- Hafner A, Lovric J, Lakos GP, Pepic I. Nanotherapeutics in the EU: an overview on current state and future directions. Int J Nanomedicine. 2014;9:1005-23.
- Hashemi B, Akram FA, Amirazad H, Dadashpour M, Sheervalilou M, Nasrabadi D, et al. Emerging importance of nanotechnology-based approaches to control the COVID-19 pandemic; focus on nanomedicine iterance in diagnosis and treatment of COVID-19 patients. Journal of drug delivery science and technology. 2022;67:102967.
- Heinz FX, Stiasny K. Distinguishing features of current COVID-19 vaccines: knowns and unknowns of antigen presentation and modes of action. NPJ vaccines. 2021;6(1):104.
- Hamimed S., Jabberi M. & Chatti A. (2022). Nanotechnology in drug and gene delivery. Naunyn Schmiedebergs Arch Pharmacol. 395(7): 769-787.
- Institute NC. Cancer nanotechnology 2022 [25/06/2022]. Available from: https://www.cancer.gov/nano/cancer-nanotechnology/detection-diagnosis.
- Li M., Li Y., Li S., Jia L., Wang H., Li M., Deng J., Zhu A., Ma L., Li W., Yu P. & Zhu T. (2022). The nano delivery systems and applications of mRNA. Eur J Med Chem. 227: 113910.
- Mattheolabakis G, Rigas B, Constantinides PP. Nanodelivery strategies in cancer chemotherapy: biological rationale and pharmaceutical perspectives. Nanomedicine (Lond). 2012;7(10):1577-90.
- Mitchell M. J., Billingsley M. M., Haley R. M., Wechsler M. E., Peppas N. A. & Langer R. (2021). Engineering precision nanoparticles for drug delivery. Nat Rev Drug Discov. 20(2): 101-124.
- Mundekkad D, Cho WC. Nanoparticles in Clinical Translation for Cancer Therapy. International journal of molecular sciences. 2022;23(3).
- Nanovax. Our recombinant, protein-based nanoparticle vaccine technology 2022 [25/06/2022]. Available from: https://www.novavax.com/science-technology/recombinant-protein-based-nanoparticle-vaccine-technology.
- Onoue S, Yamada S, Chan HK. Nanodrugs: pharmacokinetics and safety. International journal of nanomedicine. 2014;9:1025-37.
- Prabhu RH, Patravale VB, Joshi MD. Polymeric nanoparticles for targeted treatment in oncology: current insights. International journal of nanomedicine. 2015;10:1001-18.
- Shi J, Votruba AR, Farokhzad OC, Langer R. Nanotechnology in drug delivery and tissue engineering: from discovery to applications. Nano letters. 2010;10(9):3223-30.
- Smith C. C., Selitsky S. R., Chai S., Armistead P. M., Vincent B. G. & Serody J. S. (2019). Alternative tumour-specific antigens. Nat Rev Cancer. 19(8): 465-478.
- Talens-Visconti R, Diez-Sales O, de Julian-Ortiz JV, Nacher A. Nanoliposomes in Cancer Therapy: Marketed Products and Current Clinical Trials. International journal of molecular sciences. 2022;23(8).
- Thakor AS, Jokerst JV, Ghanouni P, Campbell JL, Mittra E, Gambhir SS. Clinically Approved Nanoparticle Imaging Agents. Journal of nuclear medicine : official publication, Society of Nuclear Medicine. 2016;57(12):1833-7.
- Yan Y., Liu X. Y., Lu A., Wang X. Y., Jiang L. X. & Wang J. C. (2022). Non-viral vectors for RNA delivery. J Control Release. 342: 241-279.
- Awiqli (Insulin Icodec): Giải pháp insulin nền mỗi tuần một lần dành cho bệnh nhân đái tháo đường
- Vai trò của dược sĩ trong tiêm chủng người lớn – Thực trạng, rào cản và chiến lược tiếp cận
- Ức chế PCSK9 trong dự phòng tim mạch nguyên phát – Bằng chứng mới từ thử nghiệm VESALIUS-CV
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
