Hệ mang thuốc nano được thiết kế để cung cấp các phương pháp trị liệu đã được nghiên cứu rộng rãi trong các ứng dụng y sinh và dược phẩm cho phép vận chuyển thuốc đến đích tác động, từ đó mang lại hiệu quả điều trị cao hơn. Liposome và nano polyme là hệ nano được sử dụng rộng rãi nhất cho việc vận chuyển thuốc có cấu trúc nano. Các tiểu phân nano mặc dù có khả năng mang thuốc và ổn định cao nhưng khả năng tương thích sinh học chưa cao. Ngược lại, liposome thể hiện khả năng tương thích sinh học tuyệt vời ngay cả khi chúng bị rò rỉ thuốc nhưng lại khó ổn định trong quá trình bảo quản. Để khắc phục nhược điểm của cả hai loại tiểu phân nano trên, nhiều nhóm nghiên cứu đã tập trung nỗ lực phát triển các hệ thống lai kết hợp các đặc tính mô phỏng sinh học của liposome và tính ổn định của các tiểu phân nano polyme. Trong thập kỷ qua, các tiểu phân nano polyme lai lipid này (HNPs – hybrid nanoparticles) ngày càng được xem là hệ phân phối thuốc đầy hứa hẹn do nhiều tính năng ưu việt của chúng.
Poly (acid lactic-co-glycolic) (PLGA) đã được sử dụng rộng rãi trong việc thiết kế các tiểu phân nano do tính an toàn, tính tương hợp sinh học, khả năng phân hủy sinh học và bảo vệ các phân tử thuốc khỏi bị thoái hóa. Hơn thế nữa, các sản phẩm lâm sàng được làm từ chất đồng trùng hợp này đã được phê duyệt bởi Cục Quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) để làm chất mang cho các hệ vận chuyển thuốc có cấu trúc nano. Do đó, PLGA cũng đã được nghiên cứu để phát triển hệ HNPs.
Quá trình tổng hợp tiểu phân nano PLGA chứa Fluorescein và Nile đỏ được thực hiện bằng phương pháp nhũ hóa bay hơi dung môi. Việc thu lấy tiểu phân nano được tiến hành bằng cách chuyển chất phân tán vào ống ly tâm và ly tâm ở tốc độ 25.000 vòng trong 60 phút. Sau đó, phần nổi phía trên được loại bỏ và các hạt được ngâm lại trong nước đã khử ion. Bước rửa này được lặp lại ba lần. Các tiểu phân nano (NP – nanoparticle) sau đó được phân tán lại trong dung dịch trehalose: polyme (1: 2), đông lạnh trong nitơ lỏng và đông khô trong 72 giờ.
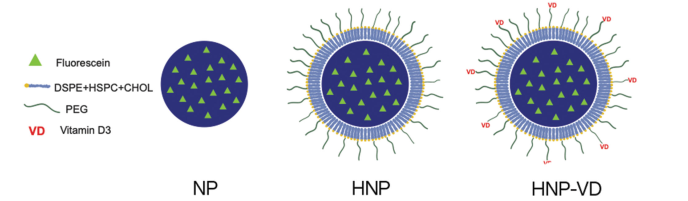
Hình 1: Tiểu phân nano chứa PLGA (NP), tiểu phân nano lai lipid- polyme (HNP), tiểu phân nano lai lipid-polyme chứa nhóm chức vitamin D3 (HNP-VD)
HNPs được tổng hợp bằng phương pháp hydrat hóa màng mỏng. Phương pháp này bao gồm sự tạo thành một màng mỏng lipid trong một bình cầu đáy tròn, sau đó hydrat hóa lớp này bằng cách phân tán các NP. Trong nghiên cứu này, các NP lai được tạo ra có và không có sự hiện diện của các phối tử nhắm mục tiêu. Một cách ngắn gọn, một hỗn hợp chất béo HSPC: CHOL: DSPE-PEG2000 (phosphatidylcholine đậu nành hydrat hóa : cholesterol : 1,2-disteroyl-sn-glycero-3-phosphaethanolamine-N-[succinyl (polyethylene glycol) – 2000) (tỷ lệ mol 2: 1: 0,1) được hòa tan trong 5 mL CHCl3. Sau đó, dung môi được làm bay hơi bằng thiết bị cô quay, tạo ra một màng lipid mỏng trên thành của bình cầu đáy tròn. Các NP đã chuẩn bị trước đó được phân tán lại trong 5 mL nước (6 mg/mL), thêm vào bình đáy tròn chứa màng lipid ở tốc độ 1 mL/phút và được siêu âm trong 10 phút. Bình đáy tròn được chuyển sang đĩa khuấy và các HNP được để yên trong 30 phút dưới sự khuấy nhẹ và sau đó được đông khô. Sự hấp thụ các hạt nano của các tế bào u hắc tố B16 được đánh giá bằng kính hiển vi huỳnh quang. Sau 3 giờ ủ với các công thức khác nhau, người ta quan sát thấy rằng có sự khác biệt trong sự phân bố tế bào của các tiểu phân nano theo công thức cụ thể của chúng (Hình bên dưới). Trong đó, NP (A) và HNP (B) nằm gần màng tế bào hơn với sự phân bố ít trong tế bào chất. Ngược lại, HNP-VD (C) có sự phân bố ở trong vùng tế bào chất và vùng khoang quanh nhân (perinuclear domain). Các hình ảnh thu được ở đây cho thấy rằng các hạt nano HNP-VD được định vị ngay cạnh nhân của các tế bào u hắc tố. Điều này cho thấy rằng các hạt nano HNP-VD có thể rất thích hợp để cung cấp các phương pháp điều trị cho nhân tế bào.
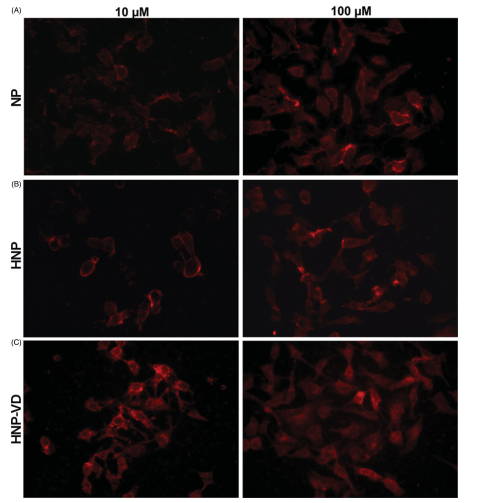
Hình 2: Hình ảnh quá trình ẩm bào của các tiểu phân nano dưới kính hiển vi huỳnh quang
Ngoài ra, sự giải phóng in vitro trong 24 giờ đầu tiên của NP, HNP và HNP-VD lần lượt là 75, 62 và 57%, tiếp theo là sự phóng thích chậm hơn trong khoảng thời gian còn lại. Những kết quả này chỉ ra rằng các chất mang nano được phát triển trong nghiên cứu này có thể được sử dụng làm hệ phân phối thuốc có kiểm soát. Hơn nữa, NP và HNP không thể hiện tác dụng đáng kể trên tế bào u hắc tố B16, tuy nhiên, HNP-VD dẫn đến sự tăng sinh tế bào, có thể là do tương tác giữa vitamin D và thụ thể của vitamin D. Dữ liệu về quá trình ẩm bào đã chỉ ra rằng HNP-VD tập trung chủ yếu ở vùng khoang quanh nhân tế bào của u hắc tố B16, có lẽ là do sự hiện diện của phối tử vitamin D nhắm vào thụ thể ở nhân tế bào. Những kết quả này khẳng định rằng HNP-VD có tiềm năng lớn cho việc phát triển các phác đồ điều trị ung thư hắc tố hướng đích cũng như phân phối đặc hiệu các chất điều trị được bao bọc đến các tế bào khác có chứa các thụ thể vitamin D ở nhân tế bào.
Tổng hợp:
Lê Hoàng Hảo
Tài liệu tham khảo:
Scopel et al, (2022), “Lipid-polymer hybrid nanoparticles as a targeted drug delivery system for melanoma treatment”, International Journal of Polymeric Materials and Polymeric Biomaterials, 71(2), 127-138.
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
- Chế độ ăn Keto có thể đẩy nhanh quá trình lão hóa cơ quan
- Một số điểm mới trong quy định giá dịch vụ khám, chữa bệnh bảo hiểm y tế giữa các bệnh viện cùng hạng trên toàn quốc từ 17/11/2023
- Si rô ngô giàu fructose thúc đẩy sự phát triển khối u đường ruột ở chuột
