Cơ chế hoạt động của vắc xin mRNA
Pfizer cũng như Moderna đều sử dụng một cách tiếp cận mới để hoạt hóa hệ thống miễn dịch của cơ thể, đó là phương pháp sử dụng mRNA (ARN thông tin). Vắc xin phòng COVID-19 chứa mRNA có khả năng kích thích tế bào trong cơ thể tạo ra phản ứng miễn dịch với vi rút gây bệnh COVID-19. Hoạt động này giúp bảo vệ cơ thể khỏi bị nhiễm bệnh COVID-19 trong tương lai. Sau khi tạo ra phản ứng miễn dịch, cơ thể sẽ tự đào thải tất cả các thành phần của vắc xin.
Để kích hoạt phản ứng miễn dịch, nhiều vắc xin đã đưa mầm bệnh yếu hoặc bất hoạt vào cơ thể, nhưng vắc xin mRNA không hoạt động như vậy. Thay vào đó, loại vắc xin này sử dụng mRNA được tạo ra trong phòng thí nghiệm để các tế bào tạo ra protein, hoặc thậm chí chỉ là một mảnh protein, và kích hoạt phản ứng miễn dịch bên trong cơ thể. Phản ứng miễn dịch đó sẽ tạo ra các kháng thể để bảo vệ cơ thể không nhiễm bệnh nếu có vi rút xâm nhập.
Cơ chế hoạt động của vắc xin mRNA cụ thể như sau: Đầu tiên, vắc xin COVID-19 mRNA được tiêm ở bắp tay trên. Từ đó mRNA sẽ xâm nhập vào các tế bào cơ và sử dụng cơ chế của tế bào để sản sinh ra mảnh vô hại của protein gai (protein gai này được tìm thấy trên bề mặt vi rút gây ra bệnh COVID-19). Sau khi sản sinh mảnh protein, các tế bào của cơ thể sẽ phá vỡ và loại bỏ mRNA. Tiếp theo, các tế bào thể hiện protein gai trên bề mặt của chúng. Hệ miễn dịch của cơ thể nhận ra protein lạ này, kích hoạt sản sinh ra các kháng thể và các tế bào miễn dịch khác để chống lại. Vào cuối quá trình này, cơ thể sẽ học được cách bảo vệ để chống lại việc nhiễm bệnh sau này do vi rút gây ra COVID-19.
Giống như tất cả các loại vắc xin, lợi ích của vắc xin mRNA trong dự phòng COVID-19 là những người được tiêm chủng có được khả năng phòng bệnh mà không phải chịu những hậu quả nghiêm trọng có thể xảy ra khi nhiễm COVID-19. Mọi cảm giác khó chịu tạm thời gặp phải sau khi tiêm vắc xin là một phần tự nhiên của quá trình và là dấu hiệu cho thấy vắc xin có tác dụng.
Sự kém ổn định của mRNA
Nhược điểm của vắc xin mRNA là dễ bị phá hủy. Nghiên cứu ban đầu về vắc xin mRNA đã chứng minh rằng mRNA trần nhanh chóng bị phân hủy sau khi sử dụng bởi ribonuclease (RNase), có nhiều trong môi trường ngoại bào. Ngoài ra mRNA còn có thể bị biến đổi về hóa học và vật lý. Sự phân hủy hóa học như thay đổi của các liên kết trong phân tử mRNA, hoặc bị mất ổn định vật lý như sự biến tính (mất cấu trúc bậc hai và bậc ba), gây ra những hậu quả khác nhau.
Sau đây là các lý do chính khiến mRNA dễ bị phá huỷ:
Một là RNA kém ổn định hơn nhiều so với DNA là do sự khác biệt quan trọng trong các loại đường tạo nên xương sống của phân tử. Xương sống của RNA là một loại đường được gọi là ribose, trong khi DNA là deoxyribose (thiếu phân tử oxy). Vì vậy DNA có thể tồn tại qua nhiều thế hệ, nhưng RNA thì tồn tại trong một thời gian ngắn hơn nhiều. Nhiều RNA sẽ nhanh chóng bị phân hủy sau khi mã hóa.
Hai là sự khác biệt về độ ổn định của các phân tử nằm ở trong cấu trúc của chúng. Các sợi kép của DNA xoắn lại thành một chuỗi xoắn kép. Nhưng RNA đi riêng lẻ thành một sợi đơn tự ghép nối với chính nó ở một số vị trí. Những “cấu trúc thứ cấp” đó có thể làm cho một số RNA trở nên mỏng manh hơn.
Ba là sự khác biệt về cấu trúc hóa học của DNA và RNA. Các nucleotide của DNA thường được biểu thị bằng các chữ cái A, T, C và G, viết tắt của adenine, thymine, cytosine và guanine. RNA cũng sử dụng A, C và G, nhưng thay cho thymine là uracil, viết tắt là U. Uracil nhô ra ngoài giống như những lá cờ vẫy chào các protein đặc biệt của hệ thống miễn dịch được gọi là các thụ thể Toll like receptor. Những protein đó giúp phát hiện RNA từ virus, chẳng hạn như SARS-CoV-2, viruscorona gây ra COVID-19 để ngăn chặn những kẻ xâm lược, đồng thời cũng khiến mRNA có thể bị phân hủy hoặc bị tấn công bởi hệ thống miễn dịch tạo ra một trở ngại cho các nhà sản xuất vắc xin. Các công ty cần đảm bảo rằng RNA vẫn còn nguyên vẹn đủ lâu để đi vào các tế bào và tạo ra các protein gai. Pfizer cũng như Moderna có lẽ đã nghiên cứu kỹ công thức hóa học của RNA để tạo ra loại vắc xin có thể vượt qua các trở ngại này. Cả hai đều đã báo cáo rằng vắc xin của họ có hiệu quả ngăn ngừa bệnh tật khoảng 95% trong các thử nghiệm lâm sàng.
Sự cải tiến để bảo vệ vắc xin COVID-19
Bước đầu tiên là sửa đổi các nucleoside mRNA để giúp chúng ổn định hơn. Ví dụ vắc xin Pfizer-BioNTech và Moderna là hai loại vắc xin có sự kết hợp nucleoside đơn lẻ của 1-methyl-pseudouridine. Một nghiên cứu trước đây đã chỉ ra rằng sự sửa đổi này cải thiện được độ ổn định của cấu trúc bậc hai RNA.
Bước tiếp theo là sử dụng các tiểu phân nano lipid để bao bọc lấy mRNA (LNPs). Đối với vắc xin Pfizer-BioNtech và Moderna, LNPs thu được bằng cách kết hợp mRNA với các thành phần lipid khác nhau bao gồm phospholipid trung tính, cholesterol, polyethylene-glycol (PEG)-lipid và lipid cation có thể ion hóa bởi có các nhóm amin và tạo điều kiện tương tác với mRNA anion trong quá trình hình thành tiểu phân và trong cả sự dung hợp với màng tế bào trong cơ thể. Ngoài ra, PEG-lipid kiểm soát kích thước hạt và hoạt động như một rào cản, ngăn ngừa sự kết tụ trong quá trình bảo quản. Khi tạo phức với mRNA, các phân tử LNPs-mRNA có kích thước trong khoảng 60-100 nm. LNPs thường được bào chế với PEG-lipid (Burke và cộng sự, 2013; Ryals và cộng sự, 2020). Các phân tử PEG ở bề mặt ngăn không cho các LNPs riêng lẻ kết hợp với nhau. Tuy nhiên, phản ứng quá mẫn quan sát thấy rõ khi tiêm bắp vắc xin mRNA-LNP COVID-19 có thể liên quan đến PEG-lipid. Do đó, các nhà khoa học đang tìm lipid khác thay thế để hạn chế tác dụng phụ này. Sự ra đời của lipid biến đổi polysarcosine đã ổn định hệ thống làm giảm phản ứng kích thích miễn dịch. Cần đánh giá bổ sung để xác định xem liệu các chất thay thế PEG-lipid như vậy có cải thiện tính ổn định của mRNA hay không.
Bên cạnh tính toàn vẹn của mRNA, sự ổn định của các LNPs rất quan trọng đối với chất lượng của vắc xin mRNA-LNPs. Không có thông tin về các đánh giá độ ổn định LNPs có thể được được tìm thấy cho vắc xin mRNA COVID-19 hiện tại, nhưng siRNA-LNP – công thức của Onpattro (Patisaran) có thời hạn sử dụng ba năm khi giữ trong khoảng từ 2oC đến 8oC. Nhìn chung, nhiều nghiên cứu chỉ ra rằng tính không ổn định của vắc xin phụ thuộc vào tính không ổn định của mRNA, chứ không phải là sự không ổn định của LNP, và nó quyết định điều kiện bảo quản, thời hạn sử dụng của vắc xin mRNA-LNP COVID-19 hiện tại.
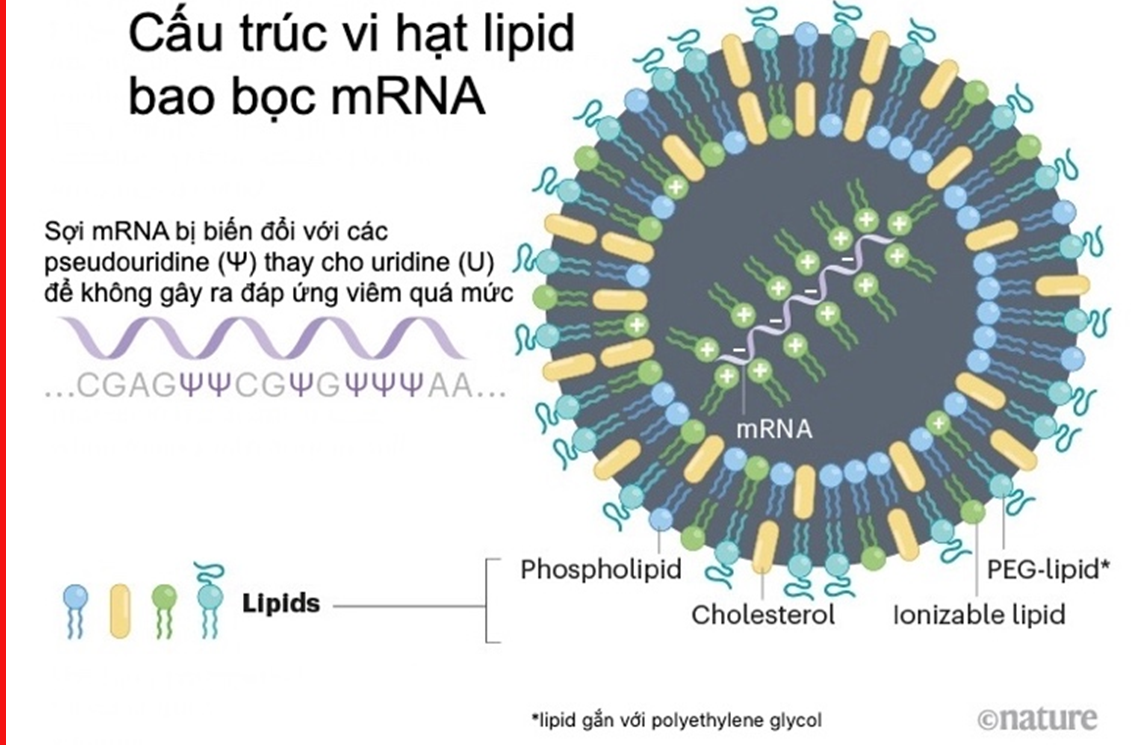
Hình: Ảnh tiểu phân nano lipid bao bọc mRNA
Nghiên cứu của các nhà khoa học chỉ ra rằng, mọi thứ diễn ra chậm hơn khi hạ nhiệt độ. Vì vậy, các phản ứng hóa học với các enzym phân hủy RNA sẽ diễn ra chậm hơn. Nó cũng giống như ý tưởng đông lạnh thực phẩm để giữ cho nó không bị hư hỏng. Do đó các vắc xin này phải bảo quản ở nhiệt thấp để có thể bảo vệ được các thành phần của vắc xin trước khi đưa vào cơ thể (vắc xin COVID-19 Mordena bảo quản ở -25oC đến -15oC, vắc xin COVID-19 bảo quản ở -80oC đến -60oC).
Tổng hợp
ThS. Lê Hoàng Hảo
Tài liệu tham khảo:
- Schoenmaker, L., Witzigmann, D., Kulkarni, J. A., Verbeke, R., Kersten, G. F. A., Jiskoot, W., & Crommelin, D. J. (2021). mRNA-lipid nanoparticle COVID-19 vaccines: structure and stability. International Journal of Pharmaceutics, 601, 120586.
- https://www.sciencenews.org/article/coronavirus-covid-19-why-vaccines-cold-freeze-pfizer-moderna (truy cập 11/10/2021)
- Awiqli (Insulin Icodec): Giải pháp insulin nền mỗi tuần một lần dành cho bệnh nhân đái tháo đường
- Vai trò của dược sĩ trong tiêm chủng người lớn – Thực trạng, rào cản và chiến lược tiếp cận
- Ức chế PCSK9 trong dự phòng tim mạch nguyên phát – Bằng chứng mới từ thử nghiệm VESALIUS-CV
- Lynkuet – thuốc mới điều trị chứng bốc hỏa do mãn kinh
- Thử nghiệm phi động vật – Kỷ nguyên mới cho nghiên cứu phát triển thuốc
- Qfitlia – phương pháp điều trị mới cho Hemophilia A hoặc B
- Mô hình “Netflix plus”: Giải pháp tài chính đột phá cải thiện tiếp cận thuốc tại các nước thu nhập thấp và trung bình
- Tỷ lệ Cholesterol “Xấu” (Non-HDL) trên Cholesterol “Tốt” (HDL) Cao Liên Quan Đến Nguy Cơ Tăng Huyết Áp và Bệnh Tim Mạch
- 6 loại thảo dược có khả năng gây tổn thương gan
- Tirzepatide giúp cải thiện tình trạng suy tim phân suất tống máu bảo tồn trên bệnh nhân béo phì
- FDA chấp thuận Ebglyss (Lebrikizumab) điều trị viêm da dị ứng
- Bệnh Alzheimer: Các loại thuốc mới được chấp thuận trên lâm sàng có tạo ra sự khác biệt thực sự không?
- FDA chấp thuận vắc-xin cúm dạng xịt mũi đầu tiên sử dụng tại nhà
- Tổn thương gan do thuốc
- Bốn hợp chất phenolic mới từ quả của loài Alpinia galanga
- Tác dụng kháng virus của gamma-mangostin
